Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1. Phản ứng giữa H2SO4 với NaOH là phản ứng
A. trung hoà B.phân huỷ C.thế D.hoá hợp
Câu 2. Dãy chất gồm những Oxít tác dụng được với axit là
A. CO2, P2O5, CaO
B.FeO, NO2, SO2
C.CO2, P2O5, SO2
D.CaO, K2O, CuO
Câu 3. Chất khi tác dụng với dung dịch HCl tạo ra một dung dịch có màu đỏ nâu là
A. Cu B.Fe C.Fe2O3 D.ZnO
Câu 4. Những nhóm oxít tác dụng được với nước là:
A. CO2, FeO, BaO B.Na2O, CaO,CO2 C.CaO, CuO, SO2 D.SO2, Fe2O3, BaO
Câu 5. Phân biệt hai dung dịch HCl và H2SO4 người ta dùng:
A. CuO B.Fe(OH)2 C.Zn D.Ba(OH)2
Câu 6. Khí SO2 được điều chế từ cặp phản ứng
A. K2SO3 và KOH
B.H2SO4 đặc, nguội và Cu;
C.Na2SO3 và HCl
D.Na2SO4 và H2SO4
Câu 7. Chất khi tác dụng với dung dịch H2SO4 tạo ra dung dịch có màu xanh lam là
A. Cu(OH)2 B.BaCl2 C.NaOH D.Fe
Câu 8: Để làm khô hỗn hợp khí CO2 và SO2 có lẫn hơi nước, người ta dùng:
A.CaO B.H2SO4 đặc C.Mg D.HCl
B.TỰ LUẬN:
Câu 1. Hãy viết PTHH thực hiện sự chuyển hóa sau:
2K+2H2O —(1)—-> 2K2O +H2
K2O+H2O—-(2)—–> 2KOH
2KOH+H2SO4—-(3)—–> K2SO4+2H2O
K2SO4+BaCl22 —(4)—–> BaSO4+2KCl
Câu 2.Trung hòa vừa đủ 500ml dung dịch Ba(OH)2 1M với dung dịch H2SO4 15%. Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng. Hãy :
a) Viết PTHH xảy ra .
b) Tính khối lượng dung dịch H2SO4 đã dùng .
c) Tính khối lượng chất kết tủa thu được.
a) \(Ba\left(OH\right)2+H2SO4-->BaSO4+2H2O\)
b) \(n_{Ba\left(OH\right)2}=0,5.1=0,5\left(mol\right)\)
\(n_{H2SO4}=n_{Ba\left(OH\right)2}=0,5\left(mol\right)\)
\(m_{H2SO4}=0,5.98=49\left(g\right)\)
\(m_{ddH2SO4}=\frac{49.100}{15}=326,667\left(g\right)\)
c) \(n_{BaSO4}=n_{Ba\left(OH\right)2}=0,5\left(mol\right)\)
\(m_{BaSO4}=0,5.233=116,5\left(g\right)\)
Câu 3.




Bài 1:
a) K: 2K + 2HCl---> 2KCl+ H2
2K + 2H2O ---> 2KOH + H2 (nếu K dư)
Zn: Zn+ 2HCl--> ZnCl2 + H2
Cu: ko có pứ
AgNO3: AgNO3+ HCl ---> AgCl + HNO3
CuO : CuO + 2HCl --> CuCl2 + H2O
NaOH: NaOH + HCl --> NaCl + H2O
Na2SO4: ko có pứ
Mg(OH)2: Mg(OH)2 + 2HCl--> MgCl2 + 2H2O
K2CO3: K2CO3 + 2HCl --- > 2KCl + CO2 + H2O
Al2O3: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
b) Na: 2Na + 2H2O --> 2NaOH
CO2: CO2 + Ba(OH)2 ---> BaCO3 + H2O (nếu Ba(OH)2 dư)
2CO2 + Ba(OH)2 ---> Ba(HCO3)2 (nếu CO2 dư)
H2SO4: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
HCl: Ba(OH)2 + 2HCl ---> BaCl2 + H2O
MgSO4: MgSO4 + Ba(OH)2 --> Mg(OH)2 + BaSO4
Al2O3: Al2O3 + 3H2SO4 --> Al2(SO4)3 + 3H2O
NaCl: ko pứ
CuCl2: CuCl2 + Ba(OH)2 ---> Cu(OH)2 + BaCl2
c) K: 2K + 2H2O --> 2KOH + H2
Mg: ko pứ
H2SO4: Na2CO3 + H2SO4 --> Na2SO4 + CO2 + H2O
KOH: ko pứ
Ca(OH)2: Ca(OH)2 + Na2CO3 --> 2NaOH + CaCO3
BaCl2: BaCl2 + Na2CO3 --> 2NaCl + BaCO3
KCl: ko pứ
Bài 2: A: Fe2O3 B: FeCl3
D: Fe(OH)3 E: Fe2O3
4Fe + 3O2 ---> 2Fe2O3
Fe2O3 + 6HCl---> 2FeCl3+ 3H2O
FeCl3 + 3NaOH --> Fe(OH)3 + 3NaCl
2Fe(OH)3 ----> Fe2O3 + 3H2O

Câu 1 :
\(a.CH_4+Cl_2\underrightarrow{as,1:1}CH_3Cl+HCl\)
\(b.C_2H_4+H_2O\underrightarrow{^{H^+,t^0}}C_2H_5OH\)
\(c.CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(d.C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(e.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(f.\left(RCOO\right)_3C_3H_5+3NaOH\rightarrow3RCOONa+C_3H_5\left(OH\right)_3\)
Câu 2 :
a) CTCT C2H2 và C2H6 :
\(CH\equiv CH\)
\(CH_3-CH_3\)
b) Nhận biết CH4, C2H4 :
Sục lần lượt các khí qua dung dịch Br2 dư :
- Mất màu : C2H4
- Không HT : CH4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
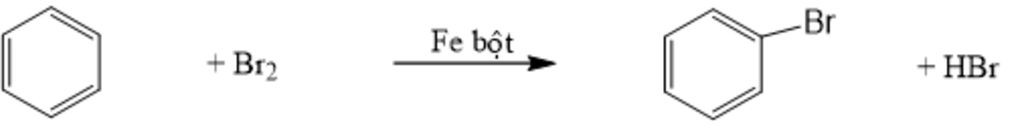
c)
TN1 : Mất màu nâu đỏ Br2 và có khí HBr thoát ra.
 TN2 :
TN2 :
Dầu ăn không tan trong nước , nổi trên bề mặt
Câu 3 :
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(n_X=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.2\left(1\right)\)
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{t^0}}CO_2+2H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{^{t^0}}2CO_2+3H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3......0.3\)
\(n_{CO_2}=a+2b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%V_{CH_4}=\%V_{C_2H_6}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Câu 4 :
\(\text{ Trong 100 ml cồn 70 độ có 70 ml rượu etylic và 30 ml nước.}\)
\(V_{C_2H_5OH}=\dfrac{70}{100}\cdot50=35\left(ml\right)\)
\(n_{C_2H_5OH}=\dfrac{9.2}{46}=0.2\left(mol\right)\)
\(n_{CH_3COOH}=\dfrac{6}{60}=0.1\left(mol\right)\)
\(CH_3COOH+C_2H_5OH\underrightarrow{H^+,t^0}CH_3COOC_2H_5+H_2O\)
\(0.1.........................0.1....................0.1\)
\(H\%=\dfrac{5.28}{0.1\cdot88}\cdot100\%=60\%\)

a.Fe + 2HCl-----> FeCl2 + H2
FeCl2 + 2NaOH----->Fe(OH)2 + 2NaCl
Fe(OH)2+ H2SO4---->FeSO4 + 2H2O
FeSO4 + Ba(NO3)2----->Fe(NO3)2 + BaSO4
b.4Al + 3O2---t*-->2Al2O3
Al2O3 + 6HCl------>2AlCl3 + 3H2O
AlCl3 + 3NaOH----->Al(OH)3 + 3NaCl
2Al(OH)3----t*---> Al2O3 + 3H2O
c.2Cu+ O2--t*->2CuO
CuO + 2HCl---->CuCl2 + H2O
CuCl2 + 2NaOH----->Cu(OH)2 + 2NaCl
Cu(OH)2---t*---> CuO + H2O
d.2Cu+ O2--t*->2CuO
CuO + 2HCl---->CuCl2 + H2O
CuCl2 + 2AgNO3-----> Cu(NO3)2 + 2AgCl
Cu(NO3)2 + 2NaOH-----> Cu(OH)2 + 2NaNO3
Cu(OH)2---t*--->CuO + H2O
CuO + H2---t*--> Cu + H2O

Câu 1: Hãy viết các PTHH theo các sơ đồ phản ứng sau đây:
1) AgNO3 + HCl ---> AgCl↓+HNO3
2) Cu + H2SO4đnóng ---> CuSO4+SO2↑+H2O
3) BaCO3 + H2SO4 ---> BaSO4+CO2+H2O
4) 2NaOH + CuSO4 ---> Na2SO4+Cu(OH)2↓
5) Al(OH)3
6) K2CO3 + 2HCl --->2KCl + CO2↑+H2O
7) Ba(NO3)2 + Na2SO4 ---> NaNO3 + BaSO4↓
8) CuSO4 + 2KOH ---> K2SO4 + Cu(OH)2↓
9) AgNO3 + HCl ---> KNO3 + AgCl↓
Câu 2: Viết PTHH thực hiện chuỗi biến hóa sau:
a. Al2O3 ---> Al ---> Al(NO3)3 ---> Al(OH)3 ---> Al2O3 ---> Al2(SO4)3 ---> AlCl3 ---> Al ---> Cu
\(2Al_2O_3--dpnc->4Al+3O_2\)
\(Al+4HNO_3-->Al\left(NO_3\right)_3+NO\uparrow+2H_2O\)
\(Al\left(NO_3\right)_3+3NaOH-->Al\left(OH\right)_3\downarrow+3NaNO_3\)
\(2Al\left(OH\right)_3-to->Al_2O_3+3H_2O\)
\(Al_2O_3+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2O\)
\(Al_2\left(SO_4\right)_3+3BaCl_2-->2AlCl_3+3BaSO_4\downarrow\)
\(3Mg+2AlCl_3-->3MgCl_2+2Al\)
\(3CuCl_2+2Al-->2AlCl_3+3Cu\)
b. Fe ---> FeCl3 ---> Fe(OH)3 ---> Fe2O3 ---> Fe ---> FeCl2 ---> Fe(NO3)2 ---> FeCO3 ---> FeSO4.
\(2Fe+3Cl_2--to->2FeCl_3\)
\(FeCl_3+3NaOH-->Fe\left(OH\right)_3\downarrow+3NaCl\)
\(2Fe\left(OH\right)_3-to->Fe_2O_3+3H_2O\)
\(Fe_2O_3+3CO-to->2Fe+3CO_2\uparrow\)
\(Fe+2HCl-->FeCl_2+H_2\uparrow\)
\(FeCl_2+2AgNO_3-->Fe\left(NO_3\right)_2+AgCl\downarrow\)
\(Fe\left(NO_3\right)_2+Na_2CO_3--->FeCO_3+2NaNO_3\)
\(FeCO_3+H_2SO_4-->FeSO_4+CO_2\uparrow+H_2O\)
c. Mg ---> MgO ---> MgCl2 ---> Mg(OH)2 ---> MgSO4 ---> MgCl2 ---> Mg(NO3)2 ---> MgCO3
\(2Mg+O_2--to->MgO\)
\(MgO+2HCl-->MgCl_2+H_2O\)
\(MgCl_2+2NaOH-->Mg\left(OH\right)_2\downarrow+2NaCl\)
\(Mg\left(OH\right)_2+H_2SO_4-->MgSO_4+2H_2O\)
\(MgSO_4+BaCl_2-->MgCl_2+BaSO_4\downarrow\)
\(MgCl_2+2AgNO_3-->Mg\left(NO_3\right)_2+2AgCl\downarrow\)
\(Mg\left(NO_3\right)_2+Na_2CO_3-->MgCO_3\downarrow+2NaNO_3\)
d. Cu(OH)2 ---> CuO ---> CuSO4 ---> CuCl2 ---> Cu(NO3)2 ---> Cu ---> CuO.
\(Cu\left(OH\right)_2-->CuO+H_2O\)
\(CuO+H_2SO_4-->CuSO_4+H_2O\)
\(CuSO_4+BaCl_2-->CuCl_2+BaSO_4\downarrow\)
\(CuCl_2+2AgNO_3-->Cu\left(NO_3\right)_2+2AgCl\downarrow\)
\(Fe+Cu\left(NO_3\right)_2-->Fe\left(NO_3\right)_2+Cu\)
\(2Cu+O_2-->2CuO\)

câu 1;
1/FeCl3 + 3NaOH => Fe(OH)3 + 3NaCl
2/ 2Fe(OH)3 --> Fe2O3 + 3H2O
3/ Fe2O3 +3 H2SO4 ==> Fe2(SO4)3 + 3H2O
4/ Fe2(SO4)3 + 6HCl ==> 2FeCl3 +3 H2SO4
5/ FeCl3 + Al ==> AlCl3 + Fe

\(M_{NO}=M_{C2H6}=30\rightarrow M_{Y'}=1,35.30=40,5,y=0,04mol\)
Gọi x,y là số mol của NO,N2O trong hh ta có hệ:
\(\begin{cases}30x+44y=0,04.40,5\\x+y=0,04\end{cases}\) \(\Rightarrow n_{NO}=x=0,01,n_{N2O}=0,03\)
Gọi a,b là số mol của Fe,R trong 3,3 gam hỗn hợp:
\(Fe+HCl\rightarrow FeCl_2+H_2\)
\(R+nHCl\rightarrow RCl_n+\frac{n}{2H2}\)
\(\Rightarrow56a+Rb=3,3\) (*)
\(\Rightarrow a+\frac{bn}{2}=0,12\) (**)
Hòa tan X trong HNO3
Quá trình oxi hóa
Fe →Fe3+ +3e
R→ Rn+ +ne
Quá trình khử:
NO3- +4H+ +3e → NO +2H2O
0,04 ← 0,03 ←0,01
NO3- +8H+ +8e → N2O +2H2O
0,3 ← 0,24 ←0,03
Áp dụng bảo toàn electron ta có
3a+ nb =0,27 (3)
Từ 2,3 → a=0,03 ,nb=0,18 thay vào 1 ta có: R=9n → n=3,R=27 → là Al
%Fe=(0,03.56/3,3).100%=50,91% → %Al = 49,09%
b, nHNO3pu =nH+ =0,04+0,3=0,34 mol
%Fe=(0,03.56/3,3).100%=50,91% → %Al = 49,09%
b, nHNO3pu =nH+ =0,04+0,3=0,34 mol
nHNO3du =0,01.0,34=0,034 mol=nH+ dư
cho NaOH vào Z
H+ + OH- → H2O
0,034→0,034
Fe3+ + 3OH- → Fe(OH)3
0,03→0,09→0,03
Al3+ + 3OH- → Al(OH)3
Al(OH)3 + OH- →AlO2- + 2H2O
Vì Fe(OH)3 kết tủa hết → nAl(OH)3 =(4,77-3,21)/78=0,02 mol < nAl3+ =0,06 mol → có 2 trường hợp
TH1 : Al3+ dư → nNaOH =0,034 +0,09 +0,06 =0,184 mol → CM(NaOH)=0,184/0,4=0,46M
TH2: Al3+ hết → nNaOH =0,034 +0,09 +0,18 +0,04 =0,344 mol → CM(NaOH)=0,344/0,4=0,86M

Ta có : + Cu không tác dụng được với dd H2SO4 loãng vì Cu đứng sau H trong dãy hoạt động hóa học.
+ CuO + H2SO4 -----> CuSO4 + H2O
+ MgCO3 + H2SO4 -----> MgSO4 + H2O + CO2
+ MgO + H2SO4 ------> MgSO4 + H2O
a/ Chất khí duy nhất có trong các phản ứng trên là CO2 nhưng khí này không cháy trong không khí. Vậy không có chất nào.
b/ Chất khí làm đục nước vôi trong là CO2 . Vậy chất cần tìm là MgCO3
c/ Dung dịch có màu xanh chính là CuSO4 , vậy chất cần tìm là CuO
d/ Dung dịch không màu chính là MgSO4 , vậy chất cần tìm là MgCO3 và MgO


1.B
2.B
Câu nào chọn C ạ