Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Xét ở 120C120C thì cứ 133,5g dd CuSO4CuSO4 bão hòa có 33,5g CuSO4CuSO4 nên có 1335g dd CuSO4CuSO4 bão hòa có số gam CuSO4CuSO4 là:
1335.33,5133,5=335(g).1335.33,5133,5=335(g).
\Rightarrow có 1000g H2O.H2O.
Gọi số gam CuSO4CuSO4 cần thêm là a.
- Xét ở 900C900C thì mCuSO4=335+amCuSO4=335+a và mH2O=1000.mH2O=1000.
\RightarrowÁp dụng CT tính độ tan ở 900C900C được S=335+a1000.100=80S=335+a1000.100=80.
\Rightarrow a = 465.

Ở 25oC , độ tan của CuSO4 là 40g có nghĩa là:
Trong 140g dd bão hòa có 40g H2O và 100g CuSO4
Vậy trong 280g dd bão hòa có x (g) H2O và y(g) CuSO4
=> x = \(\frac{280.40}{140}=80\left(g\right)\)
y = \(\frac{280.100}{140}=200\left(g\right)\)= m\(CuSO_4\)

\(PTHH:CuO+H2SO4+\text{CuSO4}+H2O\)
\(nCuO=\frac{16}{80}=0,2\left(mol\right)\)
\(\Rightarrow mH2O=0,2.18=3,6\left(g\right)\)
=>mH2SO4=0,2x98=19,6(g)
=>mddH2SO4=19,6/20%=98(g)
\(\text{Khối lượng nước có trong dung dịch H2SO4 là: 98−19,6=78,4(g)}\)
\(\text{Khối lượng nước sau phản ứng là: 78,4+3,6=82(g)}\)
Gọi khối lượng CuSO4.5H2O thoát ra khỏi dung dịch là a
\(\text{Khối lượng CuSO4 kết tinh là: 0,64a}\)
\(\text{Khối lượng CuSO4 ban đầu là: 0,2x160=32(g)}\)
Khối lượng của CuSO4 còn lại là: 32−0,64a(g)
Khối lượng nước kết tinh là: 0,36a(g)
Khối lượng nước còn lại là: 82−0,36a(g)
Độ tan của CuSO4 ở 100C là 17,4g nên ta có:
\(\text{(32−0,64a)/(82−0,36a)=17,4/100}\)
\(\Rightarrow a=30,71g\)
Tại sao khối lượng CuSO4 kết tinh lại là 0,64 g vậy ?

\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\left(1\right)\)
a_______a________a___________a
Vì H2SO4 vừa đủ nên ta có:
\(m_{H2SO4\left(bđ\right)}=98a\left(g\right)\Rightarrow m_{dd\left(H2SO4\right)bđ}=\frac{98a.100}{20}=490a\left(g\right)\)
\(\Rightarrow m_{H2O\left(dd\right)}=490a-98a=392a\left(g\right)\)
Ta có:
\(n_{CuSO4}.5H_2O=\frac{30,7}{250}=0,1228\left(mol\right)\)
\(n_{CuSO4\left(tt\right)}=0,1228\left(mol\right)\)
\(\Rightarrow n_{H2O\left(tt\right)}=0,1228.5=0,614\left(mol\right)\)
Trong dung dịch nguội còn lại 1000oC
\(m_{CuSO4}=160a-0,1228.160=160a-19648\left(g\right)\)
\(m_{H2O}=392a-0,614.18=392a-11,052\left(g\right)\)
Mà \(S_{1000^oC}=17,4\left(g\right)\)
\(\Rightarrow\frac{160a-19,648}{392a-11,052}=\frac{17,4}{100}\)
\(\Leftrightarrow160a-19,648=68,208a-1,923\)
\(\Leftrightarrow91,8a=17,725\Leftrightarrow a=0,19\)

\(CuO\left(0,2\right)+H_2SO_4\left(0,2\right)\rightarrow CuSO_4\left(0,2\right)+H_2O\left(0,2\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,2.18=3,6\left(g\right)\)
\(\Rightarrow m_{H_2SO_4}=0,2.98=19,6\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{19,6}{20\%}=98\left(g\right)\)
Khối lượng nước có trong dung dịch H2SO4 là: \(98-19,6=78,4\left(g\right)\)
Khối lượng nước sau phản ứng là: \(78,4+3,6=82\left(g\right)\)
Gọi khối lượng CuSO4.5H2O thoát ra khỏi dung dịch là x
Khối lượng CuSO4 kết tinh là: \(0,64x\)
Khối lượng CuSO4 ban đầu là: \(0,2.160=32\left(g\right)\)
Khối lượng của CuSO4 còn lại là: \(32-0,64x\left(g\right)\)
Khối lượng nước kết tinh là: \(0,36x\left(g\right)\)
Khối lượng nước còn lại là: \(82-0,36x\left(g\right)\)
Độ tan của CuSO4 ở 100C là 17,4g nên ta có:
\(\dfrac{32-0,64x}{82-0,36x}=\dfrac{17,4}{100}\)
\(\Leftrightarrow x\approx30,71\left(g\right)\)
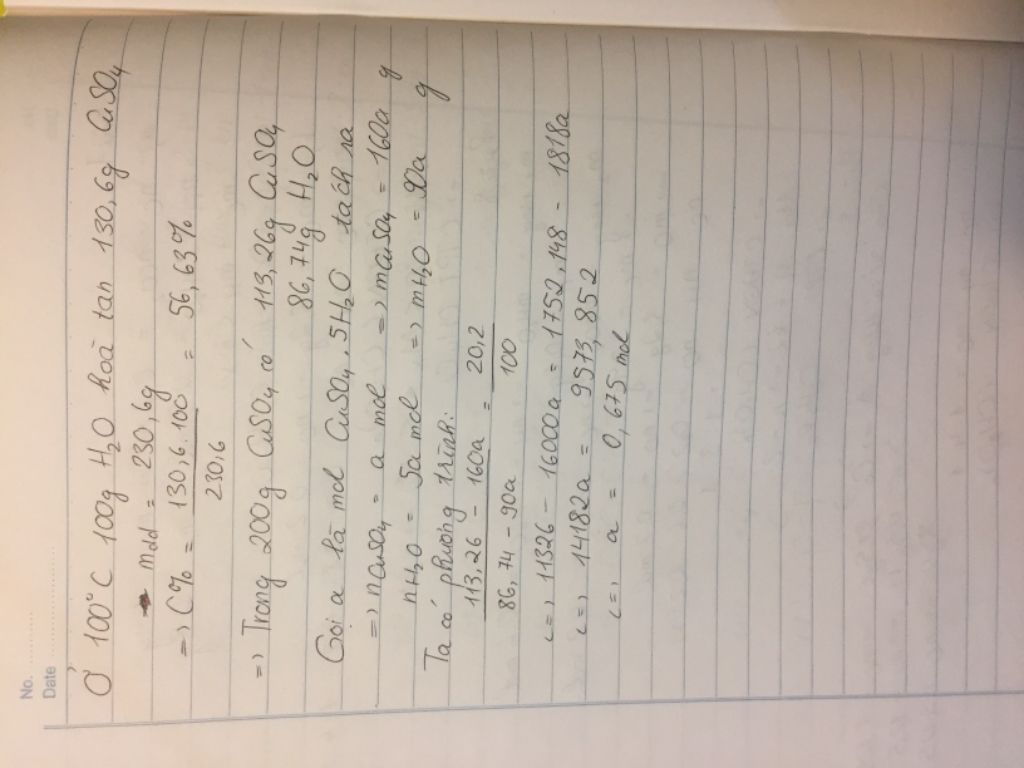
Gọi khối lượng CuSO4 ban đầu là x.
Ở 70 độ C thì 31,4 gam muối tan trong 100 gam nước tạo ra 131,4 gam dung dịch bão hòa.
Suy ra x gam muối tan tạo ra \(\frac{131,4x}{31,4}\) gam dung dịch bão hòa.
Ta có:
\(n_{CuSO4}.5H_2O=\frac{150}{160+18.5}=0,6\left(mol\right)=n_{CuSO4\left(tach.ra\right)}\)
\(\Rightarrow m_{CuSO4\left(tach.ra\right)}=0,6.160=96\left(g\right)\)
Vậy sau khi hạ nhiệt độ dung dịch còn lại x-96 gam muối.
Ở 0 độ C thì 12,9 gam muối tan trong 100 gam nước tạo ra 112,9 gam dung dịch bão hòa.
Suy ra x-96 gam muối tan tạo ra \(\left(x-96\right).\frac{112,9}{12,9}\) gam dung dịch bão hòa
BTKL,
\(\frac{131,4}{31,4}.x=150+\left(x-96\right).\frac{112,9}{12,9}\)
\(\Rightarrow x=151,117\)
\(\Rightarrow m_{dd\left(bđ\right)}=\frac{131,4}{31,4}=632,38\left(g\right)\)