Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(d_{\dfrac{A}{H_2}}=\dfrac{M_A}{M_{H_2}}=40\Rightarrow M_A=40.M_{H_2}=40.2=80\) (g/mol)
\(m_O=80.\dfrac{60}{100}=48\left(g\right)\)
\(m_S=80.\dfrac{40}{100}=32\left(g\right)\)
\(n_O=\dfrac{m}{M}=\dfrac{48}{16}=3\left(mol\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{32}{32}=1\left(mol\right)\)
\(\Rightarrow\)CTHH của khí A là SO3

Khối lượng mol của hợp chất khí là:
\(M=d,M_{H2}=8\times5,2=17\left(g/mol\right)\)
\(m_N=\dfrac{17\times82,35}{100}=14\left(g\right)\)
\(m_H=\dfrac{17\times17,56}{100}=3\left(g\right)\)
Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
\(n_N=\dfrac{m_N}{M_N}=\dfrac{14}{14}=1\left(mol\right)\)
\(n_H=\dfrac{m_H}{M_H}=\dfrac{3}{1}=3\left(mol\right)\)
\(\Rightarrow\) Công thức của hợp chất trên là: \(NH_3\)

bài 2 :
a) nhợp chất = V/22.4 = 1/22.4= 5/112 (mol)
=> Mhợp chất = m/n = 1.25 : 5/112 =28 (g)
b) CTHH dạng TQ là CxHy
Có %mC = (x . MC / Mhợp chất).100%= 85.7%
=> x .12 = 85.7% : 100% x 28=24
=> x=2
Có %mH = (y . MH/ Mhợp chất ) .100% = 14,3%
=> y.1=14.3% : 100% x 28=4
=> y =4
=> CTHH của hợp chất là C2H4
Bài 1.
- Những chất có thể thu bằng cách đẩy không khí là : Cl2,O2,CO2 do nó nặng hơn không khí
- Để thu được khí nặng hơn không khí ta đặt bình đứng vì khí đó nặng hơn sẽ chìm và đẩy không khí ra bên ngoài
- Đẻ thu được khí nhẹ hưn thì ta đặt bình úp vì khí đó nhẹ hơn cho nen nếu đặt đứng bình thì nó sẽ bay ra ngoài

Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)

M(X)= 17.2= 34(g/mol)
Gọi CTTQ của X là HxSy (x,y: nguyên, dương)
mH= 34.5,88% \(\approx\) 2(g) -> x=nH=2/1=2
mS=34-2=32(g) ->y=nS=32/32=1
=> Với x=2;y=1 -> X là H2S

câu 4
MX= 8,5.2 = 17
gọi công thức NxHy
=> x:y = \(\frac{82,35}{14}:\frac{17,65}{1}=1:3\)
=> NH3
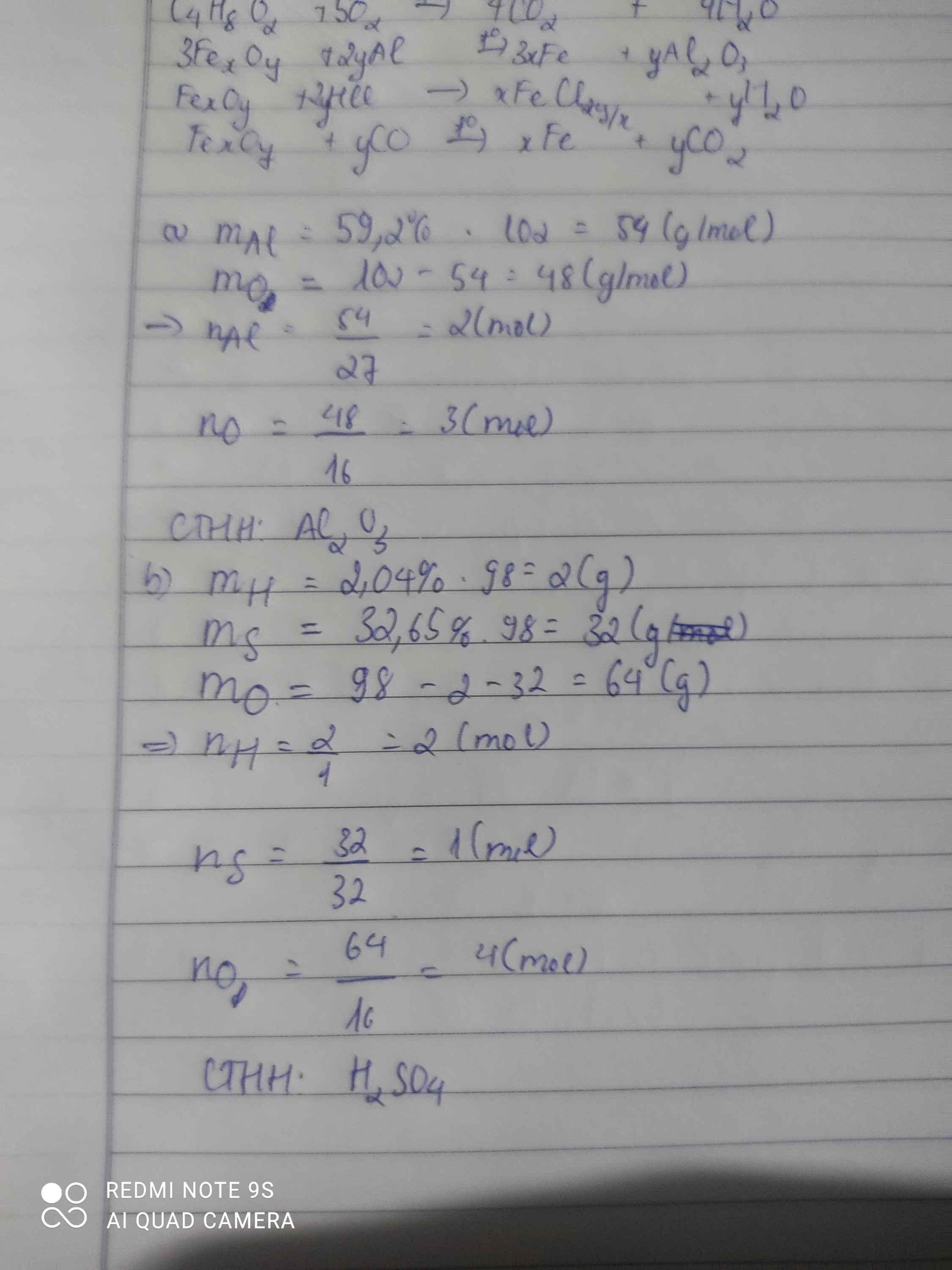
a. Gọi CTHH của hợp chất là: \(C_xH_y\)
\(d_{C_xH_y}/_{H_2}=\dfrac{M_{C_xH_y}}{M_{H_2}}=28\)
\(\Rightarrow M_{C_xH_y}=28\times M_{H_2}=28\times2=56\left(g/mol\right)\)
b. \(m_C=85,7\%.56\approx48\left(g\right)\Rightarrow n_C=\dfrac{48}{12}=4\left(mol\right)\)
\(m_H=14,3\%.56=8\left(g\right)\Rightarrow n_H=\dfrac{8}{1}=8\left(mol\right)\)
\(\Rightarrow CTHH\) của hợp chất là: \(C_4H_8\)
(%H là 14,3 % nhé bạn, không phải 143%)
Gọi CTHH của hợp chất là CxHy
a) Ta có: \(d_{\dfrac{C_xH_y}{H_2}}=\dfrac{M_{C_xH_y}}{M_{H_2}}=\dfrac{M_{C_xH_y}}{2}=28\)
\(\Rightarrow M_{C_xH_y}=28\times2=56\left(g\right)\)
b) Ta có: \(12x\div y=85,7\div14,3\)
\(\Rightarrow x\div y=\dfrac{85,7}{12}\div\dfrac{14,3}{1}\)
\(\Rightarrow x\div y=1\div2\)
Vậy CTHH đơn giản của hợp chất là (CH2)n
Ta có: \(14n=56\)
\(\Rightarrow n=4\)
Vậy CTHH của hợp chất là C4H8