Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sản phẩm oxi hoá qua bình (1) đựng dung dịch H2SO4 đặc làm khối lượng bình (1) tăng 0,63 g chính là lượng nước bị giữ lại => mH = 0,63180,6318 x 2 = 0,07 g.
Qua bình (2) chứa dung dịch Ca(OH)2 dư, làm cho bình xuất hiện kết tủa chính là do lượng CO2 bị giữ lại vì tham gia phản ứng sau:
Ca(OH)2 + CO2 → CaCO3 + H2O
0,05 51005100 = 0,05 mol
=> mC = 0,05 x 12 = 0,6 (g).
=> mO = 0,67 - (mC + mH) = 0
Từ đó tính được %mC = 89,55%; %mH = 10,45%.

Đáp án A
Đốt cháy X tạo CO2 và H2O
Bình 1 giữ lại H2O => mH2O = 7,2g => nH = 2nH2O = 0,8 mol
Bình 2 giữ lại CO2 : nCaCO3 = nCO2 = 0,3 mol
Có : mC + mH + mO = mX => nO = 0,1mol
=> nC : nH : nO = 0,3 : 0,8 : 0,1 = 3 : 8 : 1
Vậy CTĐG nhất của X là C3H8O

Đáp án B
Vì sau phản ứng, dẫn sản phẩm cháy vào bình đựng PdCl2 thấy xuất hiện kết tủa nên trong sản phẩm thu được có chứa CO:
![]()
Tiếp tục dẫn khí qua bình 2 chứa dung dịch Ca(OH)2 dư xuất hiện kết tủa nên khí bị hấp thụ là CO2 gồm CO2 tạo thành từ phản ứng (1) và có thể gồm CO2 sản phẩm cháy:
![]()
![]()
![]()

![]()
![]()
![]()


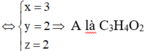

Dẫn sản phẩm cháy vào bình đựng Ca(OH)2 thì CO2 và H2O bị hấp thụ
Vì đun nước lọc thu được thêm kết tủa\(\rightarrow\) Tạo ra Ca(HCO3)2
Ca(OH)2 + CO2 \(\rightarrow\)CaCO3 + H2O
Ca(OH)2 + 2CO2\(\rightarrow\) Ca(HCO3)2
Ca(HCO3)2\(\rightarrow\)CaCO3 + CO2 + H2O
nCaCO3=\(\frac{40}{100}\)=0,4 mol
nCa(HCO3)2=nCaCO3 tạo thêm=\(\frac{25}{100}\)=0,25 mol
\(\rightarrow\)nCO2=nCaCO3 +2nCa(HCO3)2=0,9 mol
m bình tăng=mCO2 + mH2O -mCaCO3 (1) =7,7 \(\rightarrow\) mCO2 + mH2O=40+7,7
\(\rightarrow\)nH2O=8,1 gam \(\rightarrow\) nH2O=0,45 mol
\(\rightarrow\) X chứa 0,9 mol C và 0,9 mol H
Vì 0,9.12 +0,9=11,7 nên không X không chứa O
\(\rightarrow\)X có dạng (CH)n
Ta có: 70 < MX <80\(\rightarrow\) n=6\(\rightarrow\) X là C6H6
nX=\(\frac{11}{78}\)=0,15 mol
Cho X tác dụng với AgNO3 /NH3 được 43,8 gam kết tủa
\(\rightarrow\)nX=n kết tủa \(\rightarrow\) M kết tủa=292
\(\rightarrow\)Số nguyên tử Ag thế vào\(\frac{\text{292-78}}{108-1}\)=2
X có 2 liên nhóm -C≡CH
CTCT của X có thể là HC≡C-CH2-CH2-C≡CH
hoặc HC≡C-CH(CH3)-C≡CH

$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CO_2} = n_{CaCO_3} = \dfrac{12}{100} = 0,12(mol)$
Ta có : $m_{bình\ tăng} = m_{CO_2} + m_{H_2O}$
$\Rightarrow m_{H_2O} = 8,16 - 0,12.44 = 2,88(gam)$
$\Rightarrow n_{H_2O} = 0,16(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow m_O = m_X - m_C - m_H = 1,28(gam) \Rightarrow n_O = \dfrac{1,28}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,12 : 0,32 : 0,08 = 3 : 8 : 2$
Vậy CTPT của X : $(C_3H_8O_2)_n$
$M_X = 76n = M_{H_2}.38 = 76 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_2$