Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ b) n_{C_2H_4} = n_{Br_2} = \dfrac{8}{160}=0,05(mol)\\ n_{CaCO_3} = n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} = \dfrac{50}{100} = 0,5(mol)\\ \Rightarrow n_{CH_4} = 0,5 - 0,05.2 = 0,4(mol)\\ \%m_{CH_4}= \dfrac{0,4.16}{0,4.16 + 0,05.28}.100\% = 82,05\%\\ \%m_{C_2H_4} =100\% - 82,05\% = 17,95\%\)

Gọi số mol của CH4 và C2H2 lần lượt là a và b
CH4 + 2O2 ➝ CO2 + 2H2O
a 2a a
C2H2 + 2,5O2 ➝ 2CO2 + H2O
b 2,5b 2b
CO2 + Ca(OH)2 ➝ CaCO3 + H2O
a + 2b a + 2b
Số mol của hỗn hợp khí: a + b = 4,48/22,4 = 0,2 mol
Số mol kết tủa: a + 2b = 30/100 = 0,3 mol
➝ a = 0,1 mol, b = 0,1 mol
a) %VC2H2 = %VCH4 = 50%
b) Tổng số mol khí O2 đã dùng: a + 2,5b = 0,35 mol
➝ VO2 = 0,35.22,4 = 7,84 lít
➝ V kk = 5.VO2 = 39,2 lít

a) Gọi số mol CH4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{4,48}{22,4}=0,2\) (1)
\(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a--->2a----------->a
2C2H2 + 5O2 --to--> 4CO2 + 2H2O
b------>2,5b-------->2b
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,3<-----0,3
=> a + 2b = 0,3 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\%V_{CH_4}=\%V_{C_2H_2}=\dfrac{0,1}{0,2}.100\%=50\%\)
b) nO2 = 2a + 2,5b = 0,45 (mol)
=> VO2 = 0,45.22,4 = 10,08 (l)
=> Vkk = 10,08.5 = 50,4 (l)

Sửa : 29,25 \(\to\) 29,55
\(C_2H_4 + Br_2 \to C_2H_4Br_2\\ n_{C_2H_4} = n_{Br_2} = \dfrac{8}{160} = 0,05(mol)\\ \Rightarrow m_{C_2H_4} = 0,05.28 = 1,4(gam)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 +3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O\\ n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} = n_{CH_4} + 0,05.2 = n_{BaCO_3} = \dfrac{29,55}{197}=0,15(mol) \\ \Rightarrow n_{CH_4} = 0,05(mol)\\ \Rightarrow m_{CH_4} = 0,05.16 = 0,8(gam)\)
Đầu tiên, không có nước Br chỉ có nước Br2 em nhé!
---
nBr2= 8/160=0,05(mol)
PTHH: C2H4 + Br2 -> C2H4Br2
nC2H4=nBr2=0,05(mol) => mC2H4=0,05.28=1,4(g)
- Khí bay ra là khí CH4.
CH4 + 2 O2 -to-> CO2 + 2 H2O
CO2 + Ba(OH)2 -> BaCO3 + H2O
nBaCO3=29,25/197= 117/ 788 (mol ) (Số xấu quá em ơi)
=> nCH4=nCO2=nBaCO3= 117/788(mol)
=> mCH4=16. 117/788= 468/197(g)

a) Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{6,72}{22,4}=0,3\) (1)
\(n_{O_2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a--->2a----------->a
C2H4 + 3O2 --to--> 2CO2 + 2H2O
b---->3b---------->2b
=> \(2a+3b=0,8\) (2)
(1)(2) => a = 0,1; b = 0,2
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{C_2H_4}=\dfrac{0,2}{0,3}.100\%=66,67\%\end{matrix}\right.\)
b) \(n_{CO_2}=a+2b=0,5\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,5------>0,5
=> \(m_{CaCO_3}=0,5.100=50\left(g\right)\)

a) mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> \(\%V_{C_2H_4}=\dfrac{0,2.22,4}{13,44}.100\%=33,33\%\)
\(\%V_{CH_4}=100\%-33,33\%=66,67\%\)
b) \(n_{CH_4}=\dfrac{13,44.66,67\%}{22,4}=0,4\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,4--------------->0,4
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,2----------------->0,4
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,8----->0,8
=> mCaCO3 = 0,8.100 = 80 (g)
a.\(m_{tăng}=m_{C_2H_4}=5,6g\)
\(n_{hh}=\dfrac{13,44}{22,4}=0,6mol\)
\(n_{C_2H_4}=\dfrac{5,6}{28}=0,2mol\)
\(\%V_{C_2H_4}=\dfrac{0,2}{0,6}.100=33,33\%\)
\(\%V_{CH_4}=100\%-33,33\%=66,67\%\)
b.\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
0,2 0,4 ( mol )
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,4 0,4 ( mol )
\(n_{CO_2}=0,4+0,4=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 ( mol )
\(m_{CaCO_3}=0,8.100=80g\)
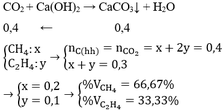
\(n_{hh}=\dfrac{V_{hh}}{22,4}=\dfrac{1,68}{22,4}=0,075mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_2\left(CH_4\right)}=x\\n_{CO_2\left(C_2H_4\right)}=2y\end{matrix}\right.\)
\(n_{CaCO_3}=\dfrac{m_{CaCO_3}}{M_{CaCO_3}}=\dfrac{10}{100}=0,1mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
x+2y x+2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}22,4x+22,4y=1,68\\x+2y=0,1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,025\end{matrix}\right.\)
\(\%CH_4=\dfrac{0,05}{0,075}.100=66,66\%\)
\(\%C_2H_4=100\%-66,66\%=33,34\%\)
\(m_{CH_4}=0,05.16=0,8g\)
\(m_{C_2H_4}=0,025.28=0,7g\)