Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
Khối lượng CaO: 
Số mol CaO:
Pt:
 số mol Ca (OH)2
số mol Ca (OH)2
Vậy khối lượng Ca(OH)2tạo thành: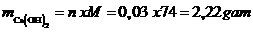
Vậy mct = 2,22 gam
 Mà
Mà 
Vậy nồng độ phần trăm Ca(OH)2: 
Câu 2:
+ Khối lượng riêng  khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 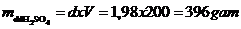
+ 
Số mol CuO: 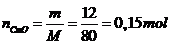
 Pt:
Pt: 

 Khối lượng
Khối lượng 
Vậy khối lượng chất tan: mct = 24 gam
Mà 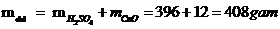
Vậy nồng độ phần trăm: 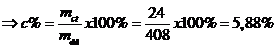

BaCl2 +H2SO4 --> BaSO4 +2HCl (1)
2NaOH +H2SO4 --> Na2SO4 +2H2O (2)
NaOH +HCl --> NaCl +H2O (3)
nBaCl2=\(\dfrac{30.20,8}{100.208}=0,03\left(mol\right)\)
nH2SO4=\(\dfrac{20.19,6}{100.98}=0,04\left(mol\right)\)
lập tỉ lệ :
\(\dfrac{0,03}{1}< \dfrac{0,04}{1}\)
=> BaCl2 hết ,H2SO4 dư => tính theo BaCl2
theo (1) :nH2SO4(pư)=nBaCl2=0,03(mol)
nHCl=2nBaCl2=0,06(mol)
=>mBaSO4=6,99(g)
mdd sau pư =30+20-6,99=43,01(g)
nH2SO4(dư)=0,01(mol)
=>mH2SO4(dư)=0,98(g)
mHCl=2,19(g)
C%dd H2SO4(dư)=2,28(%)
C%dd HCl=5,1(%)
theo (2) : nNaOH (2)=2nH2SO4(dư)=0,02(mol)
theo (3) : nNaOH (3)=nHCl=0,06(mol)
=>\(\Sigma nNaOH=0,8\left(mol\right)\)
VNaOH=0,8/5=0,16(l)=160(ml)
=> mdd NaOH=160.1,2=192(g)

a, nH2SO4=0.02*1=0.02(mol)
H2SO4 + NaOH ➞ Na2SO4 +H2O
0.02.........0.02........0.02.........0.02.......(mol)
m dung dịch NaOH=(0.02*40)*100/20=4(g)
b) H2SO4 + KOH ➞ K2SO4 +H2O
....0.02.......0.02..........0.02......0.02...(mol)
mdung dịch KOH=(0.02*56)*100/5.6=20(g)
Vdung dịch=20/1.045=19.139(ml)

II:
1. S \(\underrightarrow{\left(1\right)}\) SO2 \(\underrightarrow{\left(2\right)}\) SO3 \(\underrightarrow{\left(3\right)}\) H2SO4 \(\underrightarrow{\left(4\right)}\) Na2SO4
PTHH :
(1) S + O2 \(\underrightarrow{to}\) SO2
(2) 2SO2 + O2 \(\underrightarrow{to,V_{ }2O_{ }5}\) 2SO3
(3) SO3 + H2O \(\rightarrow\) H2SO4
(4) H2SO4 + 2NaOH \(\rightarrow\) Na2SO4 + 2H2O
(Chú ý: pt(4) bạn có thể tạo thành muối khác : FeSO4, CuSO4, ZnSO4, .....)
2. a) Hiện tượng: Vôi sống tan dần , dd trong suốt chuyển thành màu đỏ
PT: CaO + H2O \(\rightarrow\) Ca(OH)2
(dd bazơ làm dd phenolphtalein hóa đỏ)
b) H tượng: Vôi sống tan dần, giấy quỳ tím hóa xanh
PT: CaO + H2O \(\rightarrow\) Ca(OH)2
c,d) H tượng: Xuất hiện vẩn đục trắng không tan
PT: CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O
SO2 + Ca(OH)2 \(\rightarrow\) CaSO3 + H2O
e) H tượng: Giấy quỳ tím ẩm hóa đỏ
PT: SO2 + H2O \(\rightarrow\) H2SO3
f,g) H tượng: mẩu gấy tan dần, đồng thời có khí thoát ra
PT: Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
Zn + H2SO4 \(\rightarrow\) ZnSO4 + H2
h,i)H tượng: bột CuO tan hết , dd màu xanh lam
PT: CuO + 2HCl \(\rightarrow\) CuCl2 + H2O
CuO + H2SO4 \(\rightarrow\) CuSO4 + H2O
J,k) H tượng: bột FeO tan hết, dd trong suốt
Pt: FeO + 2HCl \(\rightarrow\) FeCl2 + H2O
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O
l,m) H tượng: Bột Fe2O3 tan hết, dung dịch màu vàng nâu
PT: Fe2O3 +6HCl \(\rightarrow\) 2FeCl3 + 3 H2O
Fe2O3 + 3H2SO4 \(\rightarrow\) Fe2(SO4)3 +3H2O
III:
1. nAl= \(\frac{5,4}{27}\)= 0,2 (mol)
Đổi 200ml = 0,2 l
nH2SO4 = 2 . 0,2 = 0,4 (mol)
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
ban đầu 0,2 0,4 }
pư \(\frac{2}{15}\) \(\leftarrow\) 0,4 \(\rightarrow\) \(\frac{2}{15}\) \(\rightarrow\) 0,2 } (mol)
sau pư \(\frac{1}{15}\) 0 \(\frac{2}{15}\) 0,2 }
b) Vkhí (đktc) = 0,2 . 22,4 = 4,48 (l)
c) mddH2SO4= 1,2 . 200 = 240 (g)
Áp dụng ĐLBTKL ta có:
mAl + mddH2SO4 = mdd + H2
\(\Rightarrow\) 5,4 + 240 = mdd + 0,2 . 2
\(\Leftrightarrow\) mdd = 245 (g)
C%(AlCl3) = \(\frac{\frac{2}{15}.133,5}{245}\) . 100% = 7,27 %
2.( Làm tương tự như bài 1)
Kết quả được : V = 3,36 (l)
C%(AlCl3) = 4,34%

H2SO4 + 2 NaOH ➞Na2SO4 + H2O
0.045............0.9.........................................(mol)
Do sau phản ứng làm quỳ tím chuyể màu đỏ =>còn dư axit
2KOH + H2SO4 ➞ K2SO4 +H2O
0.01.........0.005.....................................(mol)
nKOH=0.5*0.02=0.01(mol)
nH2SO4 (phản ứng với NaOH)=0.05*1-0.005=0.045(mol)
CM NaOH=0.9/0.05=1.8(M)
vậy





mNaOH = 20*20/100 = 4 (g)
nNaOH = 4/40 = 0.1 (mol)
Vdd H2SO4 = 60/1000*1.2 = 0.05 (lít)
2NaOH + H2SO4 ---> Na2SO4 + 2H2O
mol 0.1 0.05
CM H2SO4 = 0.05/0.05 = 1(M)
nFe = 16.8 /56 = 0.3 (mol)
Fe + H2SO4 ---> FeSO4 + H2
mol 0.3 0.3 0.3 0.3
CM FeSO4 = 0.3/0.2 = 1.5 (M)