Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng KCl trong 200g dd KCl 20% là:
m\(_{KCl}\)= \(\dfrac{200.20}{100}\)= 40 (g)
=> m\(_{H_2O}\)= 200 - 40 = 160(g)
Ở 30\(^o\)C:
37g KCl hòa tan trong 100g nước tạo thành dung dịch bão hòa
40g KCl____________x(g)
=> x = \(\dfrac{40.100}{37}\)= 108,108 (g)
=> Khối lượng nước bay hơi để được
dung dịch bão hòa là: 160 - 108,108 = 51,892 (g)

\(\dfrac{S}{S+100}=\dfrac{m_{ct}}{m_{bãohòa}}\Rightarrow\dfrac{35,9}{35,9+100}=\dfrac{m_{ct}}{5\cdot1000}\)
\(\Rightarrow m_{ct}=1320,824g=1,32kg\)

a) \(n_{KCl}=0,3.2=0,6\left(mol\right)\)
=> \(m_{KCl}=0,6.74,5=44,7\left(g\right)\)
b) \(m_{NaOH}=20.25\%=5\left(g\right)\)
c) \(S=\dfrac{m_{ct}}{m_{dd}}.100\)
=> \(53,6=\dfrac{m_{MgCl_2}}{100}.100\)
=> mMgCl2 = 53,6 (g)

Bài này có 2 phần phần b bị dính vô phần a mọi người thông cảm giúp

Có: \(S=\dfrac{m_{KCl}}{m_{H_2O}}.100=42,6\left(g\right)\)
=> mKCl(tan) = 106,5 (g)
=> mKCl(thừa) = 120 - 106,5 = 13,5 (g)

S=mKCl/mH2O.100=42,6(g)
=> mKCI (tan)=106,5(g)
=> mKCI ( thừa ) - 13,5 (g)

Ở 50oC có:
Cứ 100g nước hòa tan tối đa 42,6 g KCl
Cứ 250g nước hòa tan tối đa x g KCl
=> x =250.42,6100 = 106,5 g
Lượng muối còn thừa sau khi tạo thành dd bão hòa là:
muối còn thừa = 250 - 106,5 = 143,5 (g)
Bạn tham khảo ^^
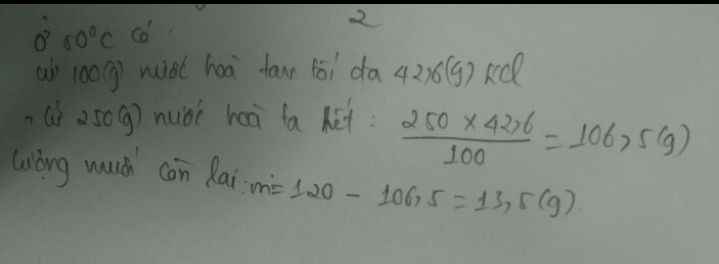
khối lượng KCl trong 200dd KCl20% là
200.20%=40 gam=> mH2O=200-40=160gam
ở 300 C
37g KCl+100g H2O-->dd bão hòa
40g KCl+x gam H2O--> dd bão hòa
=> x= 108,1gam
-> KL nước bay hơi:160-108,1=51,9gam
bạn có thể giải thích làm sao để được x=108,1 gam không?