Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
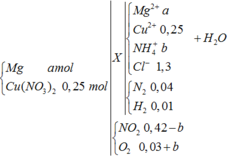
BT O : nH2O = 0,25.6 – 0,45.2 = 0,6 mol
BT H : nNH4 = ¼ (1,3 – 0,6.2 – 0,01.2) = 0,02 mol
BT ĐT : nMg = ½ (1,3 – 0,25.2 – 0,02) = 0,39 mol
Vậy m = 71,87 gam

Chọn đáp án C
Ta có ngay : 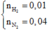 .Chú ý : Có H2 bay ra
.Chú ý : Có H2 bay ra
nghĩa là dung dịch không còn ![]()
Chúng ta hãy tư duy theo kiểu chặn đầu
với câu hỏi đơn giản nhưng quan trọng.
Clo trong HCl đi đâu? Rất nhanh có
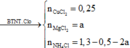 .
.
![]()
Tiếp tục, một câu hỏi nữa .0,25.3.2=1,5
mol O ban đầu đã phân bổ đi những đâu?
Nó chỉ đi vào H2O và bay lên trời
trong hỗn hợp khí (0,45 mol).
Như vậy ![]()
![]()

Chọn C.
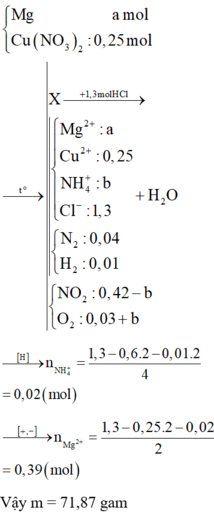
Khi nung hỗn hợp X thì :
![]()
Xét quá trình Y tác dụng với 1,3 mol HCl thì :
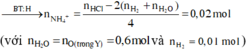
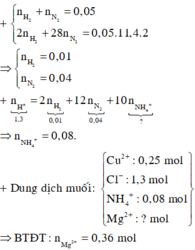
Hỗn hợp muối gồm Cu2+ (0,25 mol), Cl- (1,3 mol), NH4+ (0,02 mol) và Mg2+

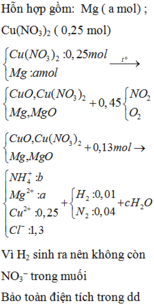
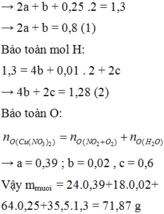



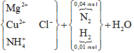

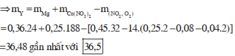

Chọn đáp án C
Đặt nN2 = x; nH2 = y ⇒ nA = x + y = 0,05 mol; mA = 28x + 2y = 0,05 × 11,4 × 2
Giải hệ có: x = 0,04 mol; y = 0,01 mol || nO/khí = 2.∑n(NO2, O2) . Bảo toàn nguyên tố Oxi:
nO/H2O = 0,25 × 6 - 0,45 × 2 = 0,6 mol. Bảo toàn nguyên tố Hidro: nNH4+ = 0,02 mol.
nCl–/Z = nHCl = 1,3 mol. Bảo toàn điện tích: nMg2+ = (1,3 - 0,25 × 2 - 0,02)/2 = 0,39 mol.
⇒ m = 0,39 × 24 + 0,25 × 64 + 0,02 × 18 + 1,3 × 35,5 = 71,87(g) ⇒ chọn C.