Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
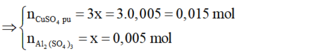

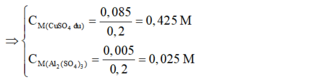
⇒ Chọn D.

\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\\ Đặt:n_{Al\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Al\left(pứ\right)}=\dfrac{3}{2}x.64-x.27=25,69-25\\ \Rightarrow x=0,01\left(mol\right)\\ \Rightarrow n_{CuSO_4\left(dư\right)}=0,2.0,5-0,01.\dfrac{3}{2}=0,085\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=0,01\left(mol\right)\\ CM_{Al_2\left(SO_4\right)_3}=\dfrac{0,01}{0,2}=0,05\left(M\right)\\ CM_{CuSO_4\left(dư\right)}=\dfrac{0,085}{0,2}=0,475M\)

a) \(m_{tăng}=32,85-16,2=16,65\left(g\right)\\3 CuSO_4+2Al\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
Gọi x là số mol Al phản ứng
=> \(n_{Cu}=\dfrac{3}{2}n_{Al}=1,5x\left(mol\right)\)
Ta có: \(m_{tăng}=1,5x.64-27x=16,65\left(g\right)\)
=> \(x=\dfrac{111}{460}\left(mol\right)\)
=> \(m_{Al\left(pứ\right)}=\dfrac{111}{460}.27=6,52\left(g\right)\); \(m_{Cu}=\dfrac{111}{460}.1,5.64=23,17\left(g\right)\)
b) \(m_{ddsaupu}=6,52+512-23,17=495,35\left(g\right)\)
\(n_{CuSO_4\left(pư\right)}=\dfrac{512.25\%}{160}=0,8\left(mol\right)\)
=> \(n_{CuSO_4\left(dư\right)}=0,8-\dfrac{111}{460}.1,5=\dfrac{403}{920}\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{111}{920}\left(mol\right)\)
=> \(C\%_{CuSO_4}=14,15\%;C_{Al_2\left(SO_4\right)_3}=8,33\%\)

Khối lượng dung dịch CuSO 4 : m dd CuSO 4 = 1,12 x 50 = 56 (gam).
CuSO 4 + Fe → FeSO 4 + Cu
64x — 56x = 5,16 - 5 = 0,16 (gam) => x = 0,02 mol.
m CuSO 4 tham gia phản ứng = 0,02 x 160 = 3,2 (gam);
100 gam dung dịch CuSO 4 có 15 gam CuSO 4 nguyên chất.
56 gam dung dịch CuSO 4 có X gam CuSO 4 nguyên chất.
x = 56 x 15/100 = 8,4g; m CuSO 4 còn lại = 8,4 - 3,2 = 5,2g
m FeSO 4 = 0,02 x 152 = 3,04g
m dd sau p / u = 56 - 0,16 = 55,84g
C % CuSO 4 = 5,2/55,84 x 100% = 9,31%
C % FeSO 4 = 3,04/55,84 x 100% = 5,44%

Gọi $n_{Fe\ pư} = a(mol)$
$Fe + CuSO_4 \to FeSO_4 + Cu$
$n_{Cu} = n_{Fe} = a(mol)$
Suy ra: $8 - 56a + 64a = 8,8 \Rightarrow a = 0,1(mol)$
$n_{FeSO_4} = n_{Fe} =a = 0,1(mol)$
$n_{CuSO_4\ dư} = 0,5.2 - 0,1 = 0,9(mol)$
$C_{M_{FeSO_4}} = \dfrac{0,1}{0,5} = 0,2M$
$C_{M_{CuSO_4}} = \dfrac{0,9}{0,5} = 1,8M$

Câu này mình trả lời rồi, bạn xem ở link sau :
https://hoc24.vn/cau-hoi/nhung-mot-la-nhom-nang-162g-vao-512g-dung-dich-cuso4-25-sau-mot-thoi-gian-lay-la-nhom-ra-khoi-dung-dich-can-lai-thay-nang-3285g-con-lai-dung-dich-aa-tinh-khoi-luong-al-da-pu-va-khoi-luong-cu.1706643518303

mddCuSO4 = 25.1,12 = 28g
⇒mCuSO4 = 4,2g
⇒nCuSO4 = 0,02625mol
Fe + CuSO4→→ FeSO4 + Cu
x →→ x-----------------x---------x
mtăng = 64x-56x = 0,08g
⇒ x=0,01mol
nFe(bđ)= 5/112 mol ⇒⇒ Fe dư, CuSO4 dư ( vì phản ứng ko hoàn toàn)
⇒⇒trong dd sau pứ có FeSO4=0,01mo; CuSO4=0,01625mol
mdd = mCuSO4 + mFepư - mCu = mddCuSO4 - mgiảm =28 - 0,08 = 27,92g
⇒ C% FeSO4 = 0,01(56 + 96).100/ 27,92 = 5,44%
C% CuSO4 = 0,01625.(64 + 96).100/27,92 = 9,31%
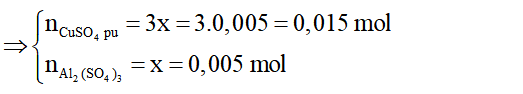
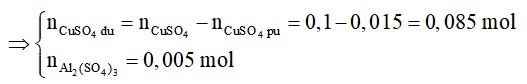
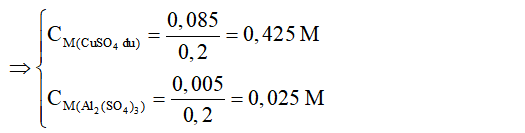

Al: 25 gam + 0,1 mol CuSO4 → thanh nhôm nặng 25,69 gam.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Sau phản ứng mtăng = 25,69 - 25 = 0,69 gam
=> \(n_{Al} = 2. \dfrac{0,69}{3 .64 - 2 . 27} = 0,01 mol\)
=> nAl2(SO4)3 = 0,005 mol; nCuSO4dư = 0,1 - 0,015 = 0,085 mol
=> CM Al2(SO4)3= 0,025 M; CM CuSO4 = 0,425 M