Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Đặt \(n_{Fe\left(phản.ứng\right)}=x\left(mol\right)=n_{Cu\left(tạo.ra\right)}\)
\(\Rightarrow64x-56x=0,8\) \(\Rightarrow x=0,1\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe\left(phản.ứng\right)}=0,1\cdot56=5,6\left(g\right)\\m_{Cu\left(tạo.ra\right)}=0,1\cdot64=6,4\left(g\right)\end{matrix}\right.\)

Zn +CuSO4= Cu +ZnSO4
Goi nZNpu=a nen nCu sinh ra=a
mthanh giam=mZn -mCu=a=0,015
CM=0,015/0,1=0,15M
Câu hỏi của pham thi hoai thanh - Hóa học lớp 8 | Học trực tuyến
Đã có bạn làm rồi, bạn vào đường link này nha!

Gọi số mol Fe phản ứng là a (mol)
PTHH: Fe + CuSO4 --> FeSO4 + Cu
a------------------->a----->a
=> 50 - 56a + 64a = 51
=> a = 0,125 (mol)
=> \(n_{FeSO_4}=0,125\left(mol\right)\)
=> \(m_{FeSO_4}=0,125.152=19\left(g\right)\)
\(Đặt:n_{Fe\left(pứ\right)}=x\left(mol\right)\\ Fe+CuSO_4\rightarrow FeSO_4+Cu\\m_{tăng}=m_{Cu}-m_{Fe\left(pứ\right)}=51-50\\ \Leftrightarrow 64x-56x=1\\ \Rightarrow x=0,125\left(mol\right)\\ n_{FeSO_4}=n_{Fe}=0,125\left(mol\right)\\ \Rightarrow m_{FeSO_4}=0,125.152=19\left(g\right)\)

Đặt số mol Fe phản ứng là x (mol)
PTHH:
Fe + CuSO4 ===> FeSO4 + Cu
x................................................x
Theo đề ra, ta có:
mkim loại tăng = mCu(bám vào) - mFe(phản ứng) = 0,8
<=> 64x - 56x = 0,8
=> x = 0,1
=> mCu(bám vào) = 0,1 x 64 = 6,4 gam

\(PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\)
\(M_{FeCl_2}=127\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow\%Fe=\dfrac{M_{Fe}}{M_{FeCl_2}}=\dfrac{56}{127}=44,09\%\)
\(\Rightarrow m_{FeCl_2}=\dfrac{m_{Fe}}{\%Fe}=\dfrac{112}{44,09\%}=254\left(g\right)\)
\(\Rightarrow n_{FeCl_2}=\dfrac{m}{M}=\dfrac{254}{127}=2\left(mol\right)\)
\(Từ.PTHH.trên:n_{HCl}=2n_{FeCl_2}=2.2=4\left(mol\right)\)
\(\Rightarrow m_{HCl}=n.M=4.36.5=146\left(g\right)\)
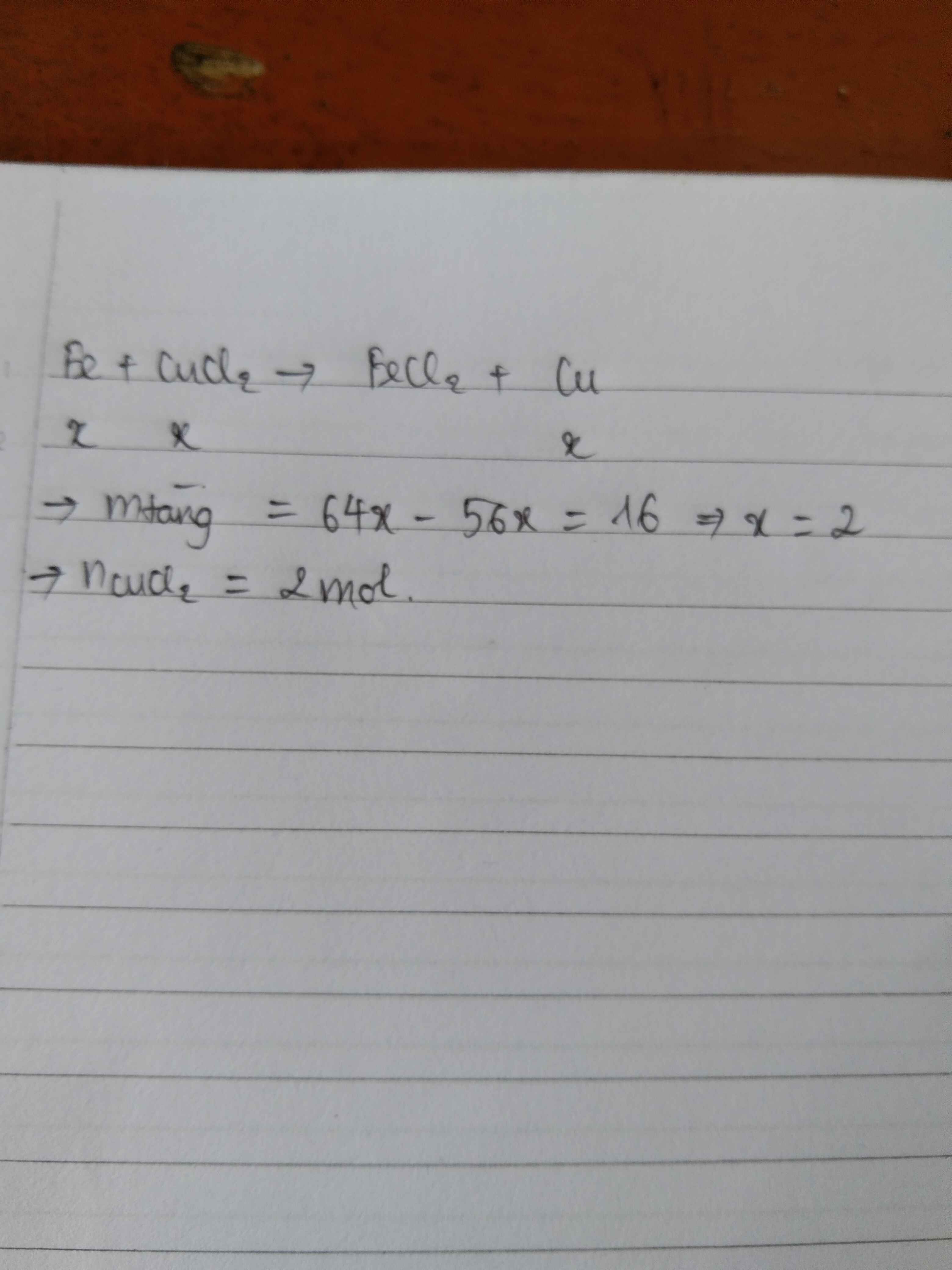
Gọi \(n_{CuSO_4} = 0,1a(mol)\\\)
\(Fe + CuSO_4 \to FeSO_4 + Cu\)
Theo PTHH :
\(n_{Cu} = n_{Fe\ pư}= 0,1a(mol) \\ \Rightarrow 64.0,1a -56.0,1a = 1,6\\ \Rightarrow a = 2(M)\\ \)
Mình hiểu r . Cảm ơn bạn nha