Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
F e + A g N O 3 0 , 03 m o l C u N O 3 2 0 , 04 m o l
Khối lượng Fe tăng m gam.
Fe + 3Ag+ → Fe2+ + 2Ag↓
Fe + Cu2+ → Fe2+ + Cu↓
Ta có:
mFe tăng = mAg + mCu - mFe phản ứng = 0,03 × 108 + 0,04 × 64 - (0,015 + 0,04) × 56 = 2,72 gam

Đáp án C.
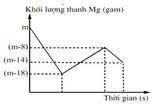
Phân tích đồ thị:
+ Đoạn 1: 3Mg + 8H+ + 2NO3- → 3Mg2+ + 2NO + 4H2O.
+ Đoạn 2: Mg + Cu2+ → Mg2+ + Cu
+ Đoạn 3: Mg + 2H+ → Mg2+ + H2
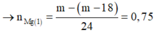
![]()
![]()
![]()

Chọn C.
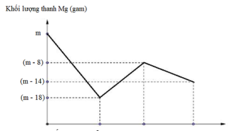
Tại thời điểm t1: thanh Mg giảm 18 gam do Mg tác dụng với H+ và NO3–
3Mg + 8H+ + 2NO3– → 3Mg2+ + 2NO + 4H2O (1)
mol: 0,75 → 2 0,5
Tại thời điểm t1 đến t2: thanh Mg tăng 10 gam do Mg đã phản ứng với Cu2+
Mg + Cu2+ → Mg2+ + Cu (2)
Ta có Dmtăng = (64 – 24).a = 10 Þ a = 0,25 mol
Tại thời điểm t2 đến t3: thanh Mg giảm 6 gam do Mg đã phản ứng với H+
Mg + 2H+ → Mg2+ + H2 (3)
Ta có mgiảm = mMg = 6 Þ nMg = 0,25 mol → 2 + 3 b = 2 + 0,5 = 2,5 mol. Vậy a : b = 1 : 10

Đáp án A.
Số mol của Cu(NO3)2 và Pb(NO3)2 trong 2 dung dịch giảm như nhau à số mol M phản ứng ở 2 thí nghiệm là như nhau.
Coi khối lượng thanh M là 10 gam.
Gọi số mol M phản ứng là x mol.
Xét thí nghiệm ở thanh 1.
M + Cu(NO3)2 à M(NO3)2 + Cu
x à x
= Mx – 64x = 0,998m = 0,02 (1)
Xét thí nghiệm ở thanh 2.
M + Pb(NO3)2 à M(NO3)2 + Pb
x à x
= 207x – Mx = 2,84 (2)
Từ (1) và (2) ta có: Mx = 1,3; x = 0,02 à M = 65 à M là Zn

Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
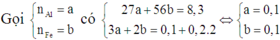
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO
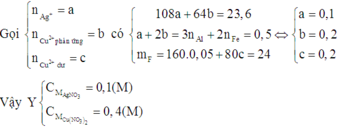

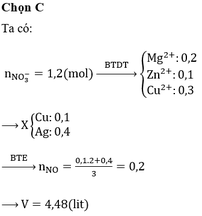
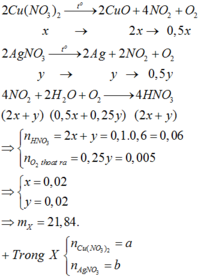
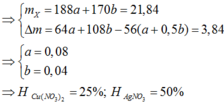
Đáp án C.
nZn = 19,5 : 65 = 0,3 mol
Zn + Cu2+ à Zn2+ + Cu
0,2ß0,2 à 0,2
Zn + Pb2+ à Zn2+ + Pb
0,1 à0,1 à 0,1
Vậy khối lượng rắn sau phản ứng là:
mrắn = mCu + mPb = 0,2.64 + 0,1.207 = 33,5 gam