Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Y công thức Oxit cao nhất là YO3 Y có hóa trị VI
Y thuộc nhóm VIA
Mặt khác Y thuộc chu kì 3 Y là S Hợp chất M là MS
M chiếm 63,64% khối lượng:
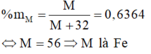

Đáp án C
Y công thức Oxit cao nhất là YO3 ⇒ Y có hóa trị VI
⇒ Y thuộc nhóm VIA
Mặt khác Y thuộc chu kì 3 ⇒ Y là S ⇒ Hợp chất M là MS
M chiếm 63,64% khối lượng:
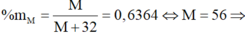 M là Fe
M là Fe

Câu 1:
Ta có
\(\frac{3}{R+3}=17,65\%\)
=>MR=14
Vậy R là Nito
Câu 2:
Ta có X có hóa trị với O gấp 3 lần hóa trị với H
=>X ở nhóm VIA
CT oxit cao nhất XO3
Ta có :
\(\text{MXO3=28}.\text{2,857=80}\)
=>MX=32
=>X là lưu huỳnh
X có Z=16
Cấu hình X:\(1s^22s^22p^63s^23p^4\)
=> X ở ô 16 chu kì 3 nhóm VIA
Câu 3:
Hợp chất với H là RH3
-->Oxit cao nhất là R2O5
Ta có :\(\frac{2R}{2R+16.5}=0,4366\)
=>R=31
->R là Photpho
Câu 4:
Y thuộc chu kỳ 3
Hợp chất oxit cao nhất là YO3 hay Y2O6
-->Y thuộc nhóm VIA
-->Y là S lưu huỳnh
->Hợp chất với kim loại là MS2
Ta có:\(\frac{M}{M+2.32}=0,4667\)
->M=56 Fe

Câu 1 : \(\%_H=\frac{3}{R+3}\cdot100=17.65\)
\(\Rightarrow R=14\)
Vậy R là N(Nitơ)
Câu 2:
Nguyên tố X có hóa trị cao nhất với Oxi gấp 3 lần so vs hc của Hidro nên X thuộc nhóm VIA
hóa trị cao nhất vs Oxi là XO3
mà tỉ khối hơi so với Nitơ là 2.875 tức MXO3 =80.5
MX=32.5
Vậy X là S(Lưu huỳnh)
1.
\(\text{% R= 100-% H= 100-17,65 = 82.35 %}\)
Ta có :
\(\frac{MR}{\%R}=\frac{MH}{\%H}\Rightarrow\frac{MR}{82,35}=\frac{3}{17,65}\)
\(\Rightarrow MR=13,99\approx14\left(đvC\right)\)
\(\rightarrow\)R là nitơ (NH3)
2.
Hóa trị của X vs oxi, hidro lần lượt là x,y
\(\Rightarrow\left\{{}\begin{matrix}\text{x + y = 8}\\\text{x =3y}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\text{x = 6}\\\text{y = 2}\end{matrix}\right.\)
Hợp chất của X vs oxi là XO3
\(\rightarrow\text{M(XO3) = 2,857.28=80}\)
\(\rightarrow\text{X = 32 }\)
\(\rightarrow\)Lưu huỳnh(S)
3.
Hợp chất của R vs Oxi là R2O5
\(\%R=\frac{2R}{\left(2R+16.5\right)}\text{= 0,4366}\)
\(\rightarrow R=31\left(\frac{g}{mol}\right)\)
\(\rightarrow\) R là Photpho
4.
Y tạo vs Oxi hợp chất YO3
\(\rightarrow\) Y tạo vs H hợp chất H2Y
Và Y ở chu kì 3\(\rightarrow\) Y là S
\(\%M=\frac{M}{\left(M+2.32\right)}\text{ = 0,4667}\)
\(\rightarrow\text{M = 56}\)
\(\Rightarrow\)M là Sắt(Fe)
Lần sau bn đăng tách câu hỏi ra cho dễ nhìn nhé



*Xác định Y:
Y thuộc chu kì 2 => Y có 2 lớp e
Công thức oxit cao nhất của Y là YO2
=> Y có hóa trị IV
=> Y thuộc nhóm IVA
=> Y có 4e lớp ngoài cùng
=> Cấu hình e của Y: 1s22s22p2
=> Y là Cacbon
*Xác định M:
Hợp chất MC2
\(\%m_C=\dfrac{2.12}{M+2.12}.100=37,5\%\)
=> M=40 (Ca)
Vậy M là Ca