Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có sơ đồ phản ứng:
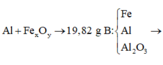
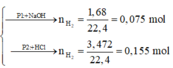
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
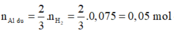
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
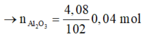
Ta có:
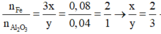
=> Oxit sắt cần tìm là Fe2O3

số mol H+ trong axit :nH+=nHCl+2nH2SO4+=V+4V=5V
- số mol H+=2nh2
- 2.0,5=5V suy ra V=0,2
- mHCl=0,2.36,5
- mH2SO4=2.0,2.98
- ap dung dinh luat bao toan khoi luong tim ra muoi

Đáp án A
Phần 1: Hỗn hợp tác dụng với HC1 gồm Al và FexOy
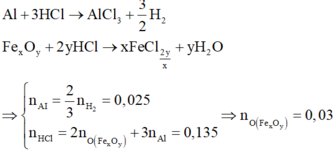
Phần 2: Có thể coi quá trình nhiệt nhôm với phản ứng xảy ra hoàn toàn như sau:

Vì phản ứng xảy ra hoàn toàn nên hỗn hợp sau phản ứng gồm Fe, A12O3 và Al dư. Khi cho hỗn hợp này vào dung dịch NaOH dư thì chất rắn còn lại là Fe.
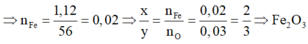

Đáp án B
Áp dụng bảo toàn electron cho các quá trình oxi hóa và khử tổng hợp từ các giai đoạn của các phản ứng.
![]()
Ta có:
![]()
Theo bảo toàn electron ta có: 4a + 0,5 = 0,9 ⇒ a = 0,1(mol)
Áp dụng định luật bảo toàn khối lượng ta có:
![]()
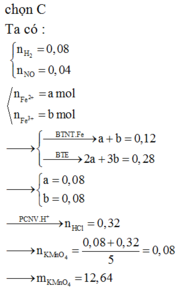
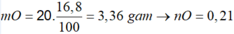
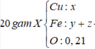
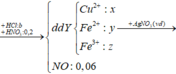
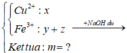
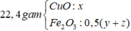
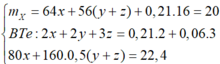
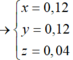
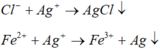
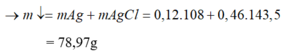

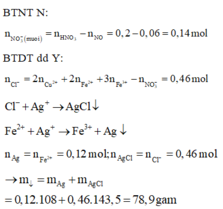
Ct oxit sat la Fe3o4
so mol O = (4.6 -3.64)/16 = 0.06
2H+ + O(2-) --> H2O
0.12 <-- 0.06 so mol H+ tham gia pu tao ra khi h2 la 0.04
Fe +2e --> Fe +2
0.02 <--0.04
2H+ +2e ---> H2 n Fe(oxit) = (3.64-0.02*56)/56 =0.045
0.04 -->0.04 CToxit = nFe(oxit ) / n (0xi) =0.045/0.06 =3/4 --- Fe3o4
mơn bạn nhìu nha