

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Giải thích:
Gọi số mol của Na và Al trong mỗi phần lần lượt là x và y mol
Nhận xét: Vì hai phần lượng khí H2 thu được chênh lệch nhau và phần 2 nhiều hơn phần 1 => ở phần 1 nhôm phản ứng dư. Mọi tính toán theo số mol của Na
Phần 1:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH + H2O → NaAlO2 + H2↑
x → 1,5x (mol)
Phần 2:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH dư + H2O → NaAlO2 + 1,5H2↑
y → 1,5y
Ta có: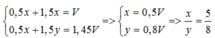
Đáp án A

Đáp án D.
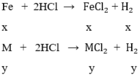
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 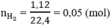
theo bài ra ta có hệ phương trình
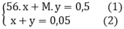
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 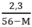
Ta có 0 < y < 0,05
y > 0 ↔ 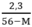 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 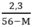 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
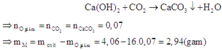
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
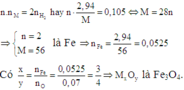
Đáp án D.