Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Dung dịch FeCl2 dễ bị không khí oxi hóa thành
muối Fe3+ . Để bảo quản FeCl2 người ta thêm 1
lương Fe vì: Fe + 2Fe3+ → 3Fe2+
Dùng HNO3 vì HNO3 oxi hóa luôn ion Fe2+ thành
Fe3+, dùng Zn sẽ tạo ra 1 lượng muối Zn2+, dùng
HCl sẽ không ngăn cản quá trình tạo Fe3+.

Đáp án D
Các thí nghiệm là: 1, 2, 4, 5, 6.
+ TN1: Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O.
+ TN2: Fe(OH)3 + 3HCl → FeCl3 + 3H2O.
+ TN3: Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O.
Fe + 2Fe(NO3)3 → 3Fe(NO3)2.
+ TN4: FeCl2 + ½ Cl2 → FeCl3.
+ TN5: Fe + 2AgNO3 → Fe(NO3)2 + 2Ag.
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag.
+ TN6: 2Fe + 3Br2 → 2FeBr3

Chọn đáp án A
Cu bị oxi hóa nghĩa là số oxi hóa của Cu tăng (có phản ứng xảy ra)
Ag không bị oxi hóa nghĩa là không có phản ứng xảy ra.
(a) cả hai đều bị oxi hóa thành oxit
(b) cả hai đều bị oxi hóa thành muối
(c) cả hai đều không phản ứng
(d) đúng vì C u + 2 F e 3 + → C u 2 + + 2 F e 2 + , Ag không phản ứng.

Đáp án A
Ta có sơ đồ phản ứng:
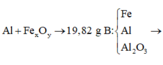
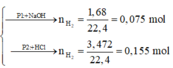
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
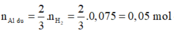
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
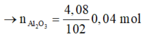
Ta có:
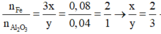
=> Oxit sắt cần tìm là Fe2O3

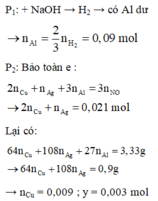
Trong 6,66g B có : 0,018 mol Cu ; 0,006 mol Ag ; 0,18 mol Al
Dung dịch C + HCl không tạo kết tủa → không có Ag+
+) Dung dịch D + thanh Fe
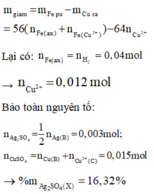
Đáp án A

Đáp án C
Hỗn hợp X gồm Ag và Cu. Thí nghiệm mà Cu bị oxi hóa còn Ag không bị oxi hóa là (d) : Cho X vào một lượng dư dung dịch FeCl3.
Phương trình phản ứng :
![]()
Ở thí nghiệm (a), cả Ag và Cu đều bị oxi hóa :
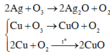
Ở thí nghiệm (b), cả Cu và Ag đều bị oxi hóa :
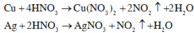
Ở thí nghiệm (d), cả Cu và Ag đều bị oxi hóa :
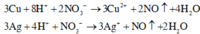

Đáp án A