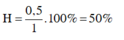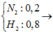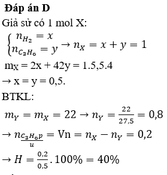Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Có MX = 7,2 => nN2 : nH2 = 1 : 4
Giả sử nN2 = 1 ; nH2 = 4 mol
N2 + 3H2 -> 2NH3
,a -> 3a -> 2a mol
=> nhh sau = 5 – 2a
Vì khối lượng khí trong bình không đổi => mX = mY
=> MX : MY = nY : nX
=> 1,8 : 2,25 = (5 – 2a) : 5
=> a = 0,5 mol
=> H% = H%N2 = 50% ( tính theo chất có H% lớn hơn)
=>A

Đáp án : A
MX = 7,2 . Áp dụng qui tắc đường chéo ta có : nH2 : nN2 = 4 : 1
=> Giả sử ban đầu có 4 mol H2 và 1 mol N2 trong X
N2 + 3H2 ↔ 2NH3
,x -> 3x -> 2x
=> sau phản ứng : nY = 2x + (1 – x) + (4 – 3x) = 5 – 2x mol
Bảo toàn khối lượng : mX = mY
=> 5.7,2 = (5 – 2x).2.4
=> x = 0,25 mol
=> H% ( tính theo N2) = 25%

MX = 8,5 . Theo qui tắc đường chéo ta có : 3n N2 = nH2 => Chọn n H2 = 3 mol => n N2 = 1 mol
Xét cân bằng: N2 + 3H2 ó 2NH3
Số mol ban đầu 1 3
Số mol phản ứng x 3x 2x Số mol cân bằng (1-x) (3-3x) 2x Số mol sau phản ứng = (4 – 2x) mol
=>dY/X = nX/nY (do khối lượng chất trong hỗn hợp không đổi)
=> 0,7.4 = 4-2x => x = 0,6 mol
=>H% = 60%
=>D

Đáp án D
► Giả sử có 1 mol X. Đặt nH2 = x; nC3H6 = y ⇒ nX = x + y = 1 mol.
mX = 2x + 42y = 1 × 5,5 × 4 ||⇒ giải hệ có: x = y = 0,5 mol.
● Bảo toàn khối lượng: mY = mX = 22(g) ⇒ nY = 22 ÷ 27,5 = 0,8 mol.
||⇒ nCH6 phản ứng = ∆n = nX – nY = 0,2 mol ||► H = 0,2 ÷ 0,5 × 100% = 40%