Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Trong 14,16 gam X chứa mN = 14,16 × 0,11864 = 1,68 gam Û nN = 0,12 mol.
Nhận thấy Hỗn hợp X chứa kim loại và gốc nitrat (NO3–).
Từ NO3 ⇒ tỉ lệ nN:nO = 1:3 ⇒ nO = 0,12×3 = 0,36 mol.
Bảo toàn khối lượng hỗn hợp X ⇒ mKim loại = 14,16 – 1,68 – 0,36×16 = 6,72 gam.
⇒ Có thể điều chế tối 6,72 gam hỗn hợp ba kim loại từ 14,16 gam X

Đáp án B
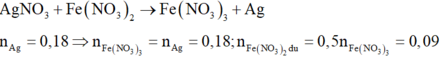
Gọi số mol Al và Mg tối đa mà dung dịch X có thể phản ứng được là x và 3x
Nên 3x + 2.3x = 0,09.2 + 0,18.3(ne cho =ne nhận)
Suy ra x = 0,08 => mAl + mMg = 7,92(g)

Đáp án C
nMg=0,3 mol; nFe=0,4 mol; nFe(NO3)3=0,5x mol; nCu(NO3)2=0,5y
Do Y gồm 2 kim loại (Cu, Fe) nên Mg hết, Fe dư, Fe(NO3)3 hết; Cu(NO3)2 hết
+ X gồm: 0,3 mol Mg(NO3)2 và a mol Fe(NO3)2
nNaOH=2nMg(NO3)2+2nFe(NO3)2=>2=2.0,3+2.a=>a=0,7mol
+ Y gồm (Cu: 0,5y mol; Fe dư: 0,5x+0,4-0,7=0,5x-0,3 mol) => 64.0,5y+56.(0,5x-0,3)=31,2 (1)
+ BTNT N: 3nFe(NO3)3+2nCu(NO3)2=2nMg(NO3)2+2nFe(NO3)2 => 3.0,5x+2.0,5y=2.0,3+2.0,7 (2)
Giải (1) và (2) => x=0,8M; y=0,8M
Giả sử chúng ta có hỗn hợp gồm 7,2 gam Mg và 22,4 gam Fe. Khi hòa tan hỗn hợp này trong dung dịch Fe(NO3)3 và Cu(NO3)2, ta thu được dung dịch X và 31,2 gam chất rắn Y gồm 2 kim loại.
Để tác dụng tối đa với dung dịch X, chúng ta cần dung dịch chứa 2,0 mol NaOH (không có không khí).
Chúng ta cần xác định giá trị của x và y.
Bước 1: Xác định số mol của Mg và Fe trong hỗn hợp ban đầu:
Số mol Mg: (n_{\text{Mg}} = \frac{{\text{khối lượng Mg}}}{{\text{khối lượng molecul Mg}}} = \frac{{7,2}}{{24,31}})Số mol Fe: (n_{\text{Fe}} = \frac{{\text{khối lượng Fe}}}{{\text{khối lượng molecu Fe}}} = \frac{{22,4}}{{55,85}})Bước 2: Xác định số mol của Fe(NO3)3 và Cu(NO3)2:
Số mol Fe(NO3)3: (n_{\text{Fe(NO3)3}} = x \times 0,5)Số mol Cu(NO3)2: (n_{\text{Cu(NO3)2}} = y \times 0,5)Bước 3: Xác định số mol của Mg(NO3)2 và Fe(NO3)2 sau phản ứng:
Số mol Mg(NO3)2: (n_{\text{Mg(NO3)2}} = n_{\text{Mg}} - n_{\text{Fe(NO3)3}})Số mol Fe(NO3)2: (n_{\text{Fe(NO3)2}} = n_{\text{Fe}} - n_{\text{Cu(NO3)2}})Bước 4: Xác định số mol của NaOH cần để tác dụng với Mg(NO3)2:
Số mol NaOH: (n_{\text{NaOH}} = 2,0)Bước 5: Xác định số mol của Mg(OH)2 sau phản ứng:
Số mol Mg(OH)2: (n_{\text{Mg(OH)2}} = n_{\text{Mg(NO3)2}})Bước 6: Tính giá trị của x:
(n_{\text{Mg(OH)2}} = n_{\text{Mg(NO3)2}})(n_{\text{Mg(OH)2}} = n_{\text{Mg}} - n_{\text{Fe(NO3)3}})(2,0 = \frac{{7,2}}{{24,31}} - x \times 0,5)Giải phương trình trên để tìm x.Bước 7: Tính giá trị của y:
(n_{\text{Cu(NO3)2}} = n_{\text{Fe}} - n_{\text{Fe(NO3)2}})(y \times 0,5 = \frac{{22,4}}{{55,85}} - x \times 0,5)Giải phương trình trên để tìm y.Sau khi tính toán, ta có:
(x \approx 0,8M)(y \approx 0,6M)Vậy giá trị của x và y là 0,8M và 0,6M

Đáp án D
có : 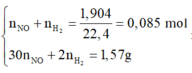
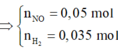
![]()
![]()
![]()
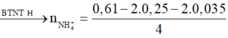
= 0,01 mol
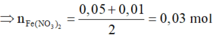
Có khí H2 thoát ra => Chứng tỏ muối sắt tạo thành là Fe2+.
Đặt số mol của Cu, Mg, Fe3O4 lần lượt là a, b, c.
![]()
![]()
![]() Kết tủa
Kết tủa
![]()
![]() (2)
(2)
![]()
![]()
![]()
=> c = 0,03 , thay vào (1), (2) suy ra
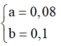
=> % m C u =
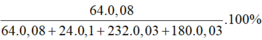
= 25,75 %

Đáp án D
Cho m gam X tác dụng với 0,61 mol HCl thu được m+16,195 gam hỗn hợp muối và 0,085 mol hỗn hợp khí Z gồm H2 và NO có tổng khối lượng là 1,57gam.
Giải được số mol H2 và NO lần lượt là 0,035 mol và 0,05 mol.
BTKL: ![]()
![]()
Bảo toàn H: 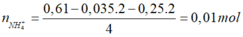
Do sinh ra khí H2 nên N O 3 - hết.
Bảo toàn N: 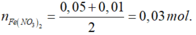
Bảo toàn O:
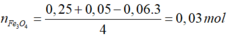
Gọi số mol Cu và Mg lần lượt là x và y.
Kết tủa thu được sẽ gồm Cu(OH)2 x mol, Mg(OH)2 y mol và Fe(OH)2 0,12 mol
→ 98x + 58y + 0,12.90 = 24,44
Do chỉ có Fe2+ nên bảo toàn e:
2x + 2y = 0,035.2 + 0,05.3 + 0,01.8 + 0,03.2 (Fe3O4)
Giải hệ: x =0,08; y = 0,1.
→%Cu = 25,75%

Đáp án D
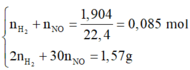
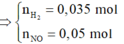
![]()
![]()

= 0,01 m0l
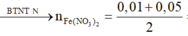
= 0,03 mol
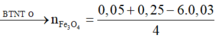
= 0,03 mol
Đặt số mol của Cu và Mg lần lượt là a, b.
![]()
![]()
![]()
![]()
![]()
⇒ % m C u =
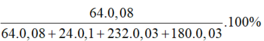
= 25,75 %



Trong 14,16 gam X chứa mN = 14,16 × 0,11864 = 1,68 gam
nN = 0,12 mol.
Nhận thấy Hỗn hợp X chứa kim loại và gốc nitrat (NO3–).
Từ NO3 ⇒ tỉ lệ nN:nO = 1:3
⇒ nO = 0,12×3 = 0,36 mol.
Bảo toàn khối lượng hỗn hợp X
⇒ mKim loại = 14,16 – 1,68 – 0,36×16 = 6,72 gam.
⇒ Có thể điều chế tối 6,72 gam hỗn hợp ba kim loại từ 14,16 gam X
Đáp án B