Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
Z có : nCO = nCO2 = 0,03 mol
=> nO pứ = nCO pứ = 0,03 mol. Đặt nO dư = a
=> Coi Y gồm Kim loại và O dư a mol
=> m = (100/25).16(a + 0,03) = 64(a + 0,03)
=> nNO3 muối = 2a + 0,04.3 = 2a + 0,12 mol
=> 3,08.64(a + 0,03) = [64(a + 0,03) – 16(a + 0,03)] + 62(2a + 0,12)
=> a = 0,118 => m = 64( 0,118 + 0,03) = 9,472g

Đáp án : A
Hỗn hợp Z gồm CO và CO2 có M = 36 dùng đường chéo => tỷ lệ mol CO = CO2 = 0,03 mol
Số mol O phản ứng = CO = 0,03 mol nên số mol O còn trong Y = (0,25m/16 - 0,03)
Khối lượng kim loại trong Y : 0,75m.
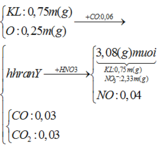
Khi phản ứng với HNO3 tạo muối có 2 loại: NO3- tạo muối thay thế O2- là 2(0,25m/16 - 0,03)(không tạo sp khử) và NO3- tạo muối có sp khử:
Số mol NO3- tạo muối tính theo NO = 0,04.3 = 0,12 mol
áp dụng BTKL: 3,08m = 0,75m + 62.0,12 + 62.2(0,25m/16 - 0,03)
=> m = 9,477 gần giá trị 9,5.
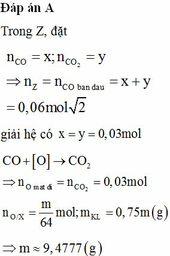
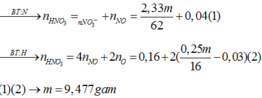


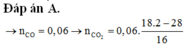
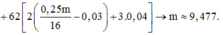
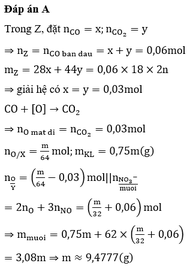
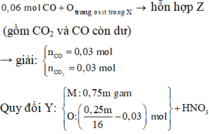

Theo giả thiết: mO = 0.25a (g) => mKL = 0.75a (g);
=> nO = 0.25a/16 mol. nZ = nCO = 1.344/22.4 = 0.06 mol.
M (Z gồm CO & CO2)
Mz = 18*2 = 36 => nCO = nCO2 = 0.03 mol
=> nO pư( nguyên tử) = 0.03 mol => nO còn lại = 0.25a/16 -0.03 mol
Từ khối lượng muối = 3.08a => mNO3(-) = 3.08a - 0.75a = 2.33a (g).
Từ nNO = 0.04 => nNO3( trong muối) = 0.04*3 = 0.12 mol( ĐCGĐ)
Lượng NO3 tạo từ oxi: nNO3/oxit = 2.33a/62 - 0.12 mol
Từ đó suy ra: nNO3/oxit = 2* nO(còn lại) <=>2* (2.33a /62 - 0.12) = 0.25a/16 - 0.03 => a = 9.4777
=> Đáp án C