Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Chất rắn m1 là Cu. Bảo toàn e có 2nCu=3nNO
→ 2b = 2V/70
Gọi số mol: Mg là x; Cu là y; Al là z và NH4NO3 là t
Ta có hệ phương trình
(1) 2x +3y = 2n(H2) = 0,88
(2) 24x + 64y + 27z = 19,92
(3) 148x + 188y + 213z + 80t = 97,95
(4) 2x + 2y + 3t = 3n(NO) + 8n(NH4NO3) = 3V/22,4 + 8t = 6,25y + 8t
→ x = 0,08; y = 0,18; z = 0,24
→ %Mg = 9,64%

Đáp án C
X + CO tạo thành chất rắn Y gồm các kim loại Mg, Fe, Cu và hỗn hợp khí z gồm CO2 và CO dư
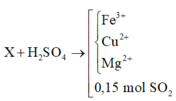
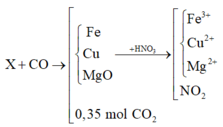
Áp dụng định luật bảo toàn mol electron
Trong thí nghiệm 1: ne nhường = ne nhận = 0,3(mol)
ne nhường trong thí nghiệm = ne nhường (1) + 2.nCO2 =1(mol) = ne nhận (2) = nNO2
Chú ý: Với các bài toán của phản ứng oxi hoá khử gồm nhiều quá trình ta thường sử dụng bảo toàn electron cho toàn bộ các quá trình, bỏ qua giai đoạn trung gian.

Đáp án A
m X = 136a => m O = 11,36 => n O = 0,71 mol
Quy đổi hỗn hợp X về a mol Mg, 2a mol Fe và 0,71 mol O.
Y tác dụng với HNO3 dư tạo ra khí NO, N2O và dung dịch chứa muối NH4NO3.
Cô cạn dung dịch thu được rắn chứa a mol Mg(NO3)2 , 2a mol Fe(NO3)3 và NH4NO3.
→ n N H 4 N O 3 = 0 , 1875 a
Do vậy số mol NO và N2O đều là 0,1875a.
Bảo toàn e: 2a + 2a.3 = 0,71.2 + 0,1875a.3 + 0,1875a.8 + 0,1875a.8
Giải được: a=0,32.
Đốt hỗn hợp X bắng Cl2 và O2 thu được Z.
Hòa tan Z cần 1,6 mol HCl → n O = 0 , 8 → n O 2 = 0 , 4
Gọi số mol Cl2 là x , kết tủa thu được là AgCl 2x +1,6 và Ag.
Bảo toàn e: n A g = 0,32.2 + 0,64.3 - 0,8.2 - 2x = 0,06 - 2x
=> 108(0,96 - 2x) + (108 + 35,5)(2x + 16) = 354,8
Giải được: x=0,3.
=> V = (0,3 + 0,4).22,4 = 15,68

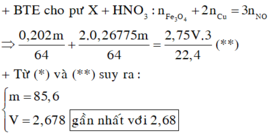

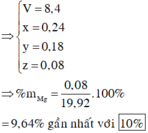

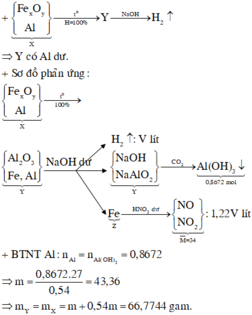

Đáp án B