Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Sử dụng sơ đồ đường chéo ⇒ nO2:nO3 = 5:3
+ Giả sử nCO2 6 mol và nH2O = 7 mol ta có sơ đồ.
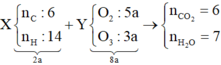
+ Bảo toàn Oxi ⇒ 2nO2 + 3nO3 = 5x2a + 3x3a = 2nCO2 + nH2O = 6x2 + 7 = 19 ⇒ a = 1
![]()
⇒ Chọn C

a) Khí A có khối lượng = 0,25.64 = 16; Gọi A có công thức CxHy, vì C chiếm 75% nên 12x/y = 75/25 ---> x/y = 1/4.
Vậy A có CTHH: CH4 (metan).

a) MA= 64 . 0,25 = 16 g/mol
gọi CTC của A là CxHy
Ta có : \(\frac{12x}{y}=\frac{75\%}{25\%}\)=> \(\frac{x}{y}=\frac{75}{25.12}=\frac{75}{300}=\frac{1}{4}\)
CTHH : CH4

Chọn đáp án C
50 mL khí không bị ngưng tụ là C O 2 ; tỉ lệ n H 2 O : n C O 2 = 4 : 5
→ có 40 mL H 2 O
các khí và hơi đo ở cùng điều kiện nhiệt độ, áp suất → chọn điều kiện V = 10 mL ⇄ 1 mol.
Ta có: đốt 1 mol este X cần 5 m o l O 2 → t 0 5 m o l C O 2 + 4 m o l H 2 O
BTNT oxi có trong X: n O = 4
→ số O = 4 : 1 = 4.
Lại có số C = 5 : 1 = 5 và số H = 4 × 2 : 1 = 8
→ CTPT của X là C 5 H 8 O 4
Tính được MX = 132

Đáp án D
• hhX gồm nCnH2n + 2 = 1,68 : 22,4 = 0,075 mol;
Đốt cháy 0,075 mol CnH2n + 2; 0,05 mol CmH2m+2–2a → 0,225 mol CO2
Số C trung bình = 0,225 : 0,125 ≈ 1,8 → Ankan là CH4.
Ta có: nCO2 = 0,075 + 0,05m = 0,225 → m = 3
Nhận thấy nBr2 pứ = 2nCmH2m+2–2a ⇒ CxHy còn lại có a = 2 Û CmH2m–2
Û C3H4

Chọn đáp án C

=> có một khí là CH4 ⇒ n C H 4 = 1 , 12 22 , 4 = 0 , 05 (mol)
=> số mol khí còn lại trong X là : 0,075 – 0,05 = 0,025 (mol) = nBr2
=> Gọi CTPT của anken là CnH2n: 0,025 (mol)
BTNT C => 0,025n + 0,05 = 0,125
=> n = 3 => C3H6
Vậy hỗn hợp X gồm CH4 và C3H6
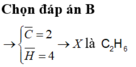


Đáp án C