Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dạng bài KL có tính khử mạnh như Al, Mg… tác dụng với HNO3 (hoặc H2SO4) cần chú ý sản phẩm có thể có muối NH4NO3.
- Ta có hệ:
nN2 + nN2O = 0.24 mol
28nN2 + 44nN2O = 0.24*18*2 g
=> nN2 = 0.12 mol; nN2O = 0.12 mol
- Bảo toàn electron cho phản ứng:
3nAl = 10nN2 + 8nN2O + 8nNH4NO3
=> 3*m/27 = 10*0.12 + 8*0.12 + 8*nNH3NO3
=> nNH3NO3 = m/72 – 0.27 (mol)
- Khối lượng muối tạo thành: mmuối = mAl(NO3)3 + mNH3NO3
=> 8m = 213*(m/27) + 80*( m/72 – 0.27)
=> m = 21.6 g
=> Đáp án D

Đáp án B
nAl = m/27 => mAl(NO3)3 = 213.m/27 = 71m/9 < 8m
=> mNH4NO3 = 8m – 71m/9 = m/9 => nNH4NO3 = m/720

Bảo toàn ne => 3nAl = 10nN2 + 8nN2O + 8nNH4NO3
=> 3m/27 = 10.0,12 + 8.0,12 + 8m/720 => m = 21,6

Chọn đáp án D
MX = 18×2 = 36 ⇒ mX = 8,64 gam.
⇒ Lập hệ pt có: nN2O = nN2 = 0,12 mol.
Đặt nAl = x mol ⇒ Bảo toàn e có: 3nAl = 8nNH4NO3 + 10nN2 + 8nN2O
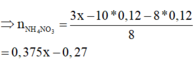
⇒ mMuối = mAl(NO3)3 + mNH4NO3 = 213x + 80×(0,375x – 0,27) = 243x – 21,6.
+ Vì mMuối = 8mAl ⇒ 243x – 21,6 = 8×27x ⇒ x = 0,8 mol
⇒ m = 27×0,8 = 21,6 gam ⇒ Chọn D



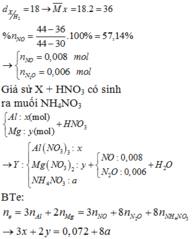
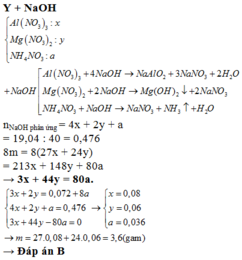
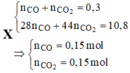
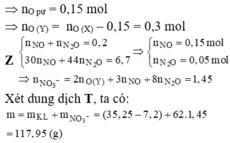
Đáp án B