Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có sơ đồ phản ứng :
FeS2, Cu2S+ HNO3 →Fe2(SO4)3+ CuSO4+ NO+ H2O
Bảo toàn nguyên tố Fe ta có: nFe2(SO4)3= 1/2. nFeS2= 0,12/2= 0,06 mol
Bảo toàn nguyên tố Cu ta có: nCuSO4= 2.nCu2S= 2 a mol
Bảo toàn nguyên tố S có nS( FeS2, Cu2S)= nS (trong 2 muối sunfat)
Nên 2.0,12+ a= 3.0,06+ 2a→ a= 0,06 mol
Đáp án D

Ta có sơ đồ phản ứng :
FeS2, Cu2S+ HNO3 →Fe2(SO4)3+ CuSO4+ NO2+ H2O
Bảo toàn nguyên tố Fe ta có: nFe2(SO4)3= 1/2. nFeS2= 0,01/2= 0,005 mol
Bảo toàn nguyên tố Cu ta có: nCuSO4= 2.nCu2S= 2 y mol
Bảo toàn nguyên tố S có nS( FeS2, Cu2S)= nS (trong 2 muối sunfat)
Nên 2.0,01+ y= 3.0,005+ 2y → y=0,005 mol
QT cho e :
FeS2 → Fe3++ 2S+6+15 e
Cu2S → 2Cu2++ S+6+ 10e
Tổng số mol e cho là
ne cho= 15.nFeS2+ 10. nCu2S = 15.0,01+10.0,005=0,2 mol
QT nhận e :
N+5+ 1e → NO2
0,2→ 0,2 mol
Theo ĐL BT e : ne cho= ne nhận= 0,2 mol →V= 4,48 lít
Đáp án C

Thu được hai muối sunfat là \(Fe_2\left(SO_4\right)_3\) và \(CuSO_4\)
\(FeS_2\rightarrow Fe^{+3}+2S^{+6}+15e\)
a a 2a 15a
\(Cu_2S\rightarrow2Cu^{+2}+S^{+6}+10e\)
0,06 0,03 0,06 0,6
BTĐT: \(3n_{Fe^{3+}}+2n_{Cu^{2+}}=2n_{SO_4^{2-}}\)
\(\Rightarrow3a+2\cdot0,03=2\cdot\left(a+0,06\right)\)
\(\Rightarrow a=0,06mol\)
\(Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_3+3BaSO_4\)
0,06 0,18
\(CuSO_4+BaCl_2\rightarrow CuCl_2+BaSO_4\)
0,06 0,06
\(m_{\downarrow}=\left(0,18+0,06\right)\cdot233=55,92g\)

-Coi X là hỗn hợp của Fe và O2
\(n_{Fe}=\dfrac{m}{M}=\dfrac{8,4}{56}=0,15mol\)
\(n_{O_2}=xmol\)
\(n_{NO_2}=\dfrac{v}{22,4}=\dfrac{2,24}{22,4}=0,1mol\)
Fe\(\rightarrow Fe^{3+}+3e\)
0,15\(\rightarrow\)............0,45
O2\(+4e\rightarrow2O^{-2}\)
x\(\rightarrow\)4x
\(N^{+5}+1e\rightarrow N^{+4}\)
..............0,1\(\leftarrow\)0,1
-Bảo toàn e: 4x+0,1=0,45\(\rightarrow\)4x=0,35\(\rightarrow\)x=0,0875mol
\(m=m_{Fe}+m_{O_2}=8,4+0,0875.32=11,2gam\)

nAl = nAl(NO3)3 = 3,78/27 = 0,14 mol
mAl(NO3)3 = 0,14.213 = 29,82 g < 31,42
=> m muối bao gồm Al(NO3)3 và NH4NO3
m NH4NO3 = 31,42 - 29,82 = 1,6 g
n NH4NO3 = 1,6/80 = 0,02 mol
bảo toàn điện tích 3nAl = 8nN20 + 3nNO + 8nNH4NO3
=) 8nN20 + 3nNO = 0,26
ta có 6nN2O - nNO = 0
giải hệ trên ta đc \(\left\{{}\begin{matrix}nN2O=0,01mol\\nNO=0,06mol\end{matrix}\right.\)
=> a= 0,01 + 0,06 = 0,07 mol

Chọn A
Quy đổi hỗn hợp X thành: Ba (x mol); K (y mol); Al (z mol) và O (t mol)
→ m O = 16t = (137x + 39y + 27z + 16t).10% → 13,7x + 3,9y + 2,7z - 14,4t = 0 (1).
Bảo toàn electron có: 2x + y + 3z = 2t + 0,056.2 → 2x + y + 3z – 2t = 0,112 (2)
Theo bài ra kết tủa gồm
BaSO
4
: x mol và
Al
(
OH
)
3
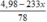 mol
mol
Dung dịch X gồm:
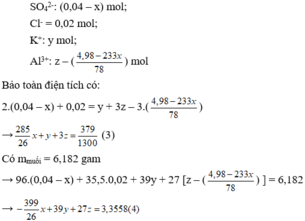
Từ (1); (2); (3) và (4) có x ≈ 0,012; y ≈ 0,076; z ≈ 0,03; t ≈ 0,036.
Vậy m = 0,012. 137 + 0,076.39 + 0,03.27 + 0,038.16 ≈ 6 (gam).

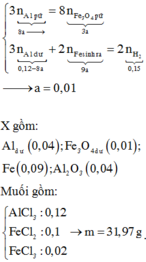

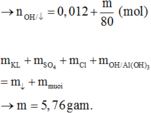
Chọn đáp án B