Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(R+2HCl\rightarrow RCl_2+H_2\)
0,2 0,2
\(\Rightarrow\overline{M_R}=\dfrac{4,8}{0,2}=24đvC\)
Vậy kim loại R là Mg.
Muối thu được là \(MgCl_2\) có khối lượng là:
\(m_{MgCl_2}=0,2\cdot95=19g\)

Thể tích khí đưa vào quả bóng: V1 = N.ΔV = 45.0,1 = 4,5 l
Áp dụng Định luật Bôi-lơ-Ma-ri-ôt:
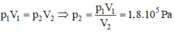

45 lần bơm đã đưa vào quả bóng một lượng khí ở bên ngoài có thể tích và áp suất tương ứng là:
V1 = 45. 125 cm3 = 5625 cm3
P1 = 105 Pa
Khi nhốt hết lượng khí trên vào quả bóng thì nó có thể tích là bằng thể tích quả bóng:
V2= 2,5 lít = 2500 cm3
và một áp suất là P2
Quá trình là đẳng nhiệt, áp dụng công thức định luật Bôi-lơ-Ma-ri-ốt:
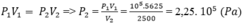

Nhiệt lượng tỏa ra:
Q K l = m K l . C K l t 2 − t = 0 , 4. C K l . 100 − 20 = 32. C K l
Nhiệt lượng thu vào:
Q t h u = Q H 2 O = m H 2 O . C H 2 O t − t 1 = 10475 J
Ta có:
Q t o a = Q t h u ⇔ 32 C K l = 10475 ⇒ C K l = 327 , 34 J / K g . K
Đáp án: A

Ta có:
Qtoa là nhiệt lượng mà sắt tỏa ra
Qthu là nhiệt lượng mà nước và nhôm nhận được để tăng nhiệt độ lên 800C và nhiệt lượng của 5g nước tăng từ 200C lên 1000C rồi hóa hơi
Khi quả cầu bắt đầu chạm vào m1=5g nước đã bốc hơi nên lượng nước tăng từ 200C lên 800C chỉ có
m′ = 100 − 5 = 95g
+ Q t o a = m F e c F e t - 80
+ Q t h u = m A l c A l 80 - 20 + m ' c n c 80 - 20 + m 1 c n c 100 - 20 + m 1 L
Theo phương trình cân bằng nhiệt, ta có:
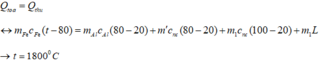
Đáp án: A

a)\(n_{HCl}=0,5\cdot1=0,5mol\)
PT: \(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(n_R=\dfrac{4,05}{M_R}\)
\(n_{H_2}=\dfrac{5,04}{22,4}=0,225mol\)
\(\Rightarrow\dfrac{4,05}{M_R}\cdot n=0,225\cdot2\)
R là kim loại:
\(\begin{matrix}n&1&2&3\\M_R&9&18&27\end{matrix}\)
Vậy R có hóa trị III và \(M_R=27\left(Al\right)\)
b)PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,15 0,5 0,225
0,15 0,45 0,15 0,225
Vậy \(C_{M_{AlCl_3}}=\dfrac{0,15}{0,5}=0,3M\)