Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nFeCl2 = nH2 = 0,1mol; nKMnO4 = 0,025 mol
Fe2+ sẽ phản ứng trước với KMnO4 / H+, mà thu được khí clo nên Fe2+ đã phản ứng hết, tiếp là Cl-
Bảo toàn e: nFe2+ + nCl- (pư) = 5.nMn+7
⇒ nCl- (pư) = 0,025 .5 – 0,1 = 0,025
nFe2+ + nCl- (pư) = 5.nMn7+ ⇒ nCl- (pư) = 0,025 .5 – 0,1 = 0,025 mol
⇒ nCl2 = 0,0125 mol ⇒ VCl2 = 0,28l

n H2=\(\dfrac{1,456}{22,4}\)=0,065 mol
ta có : m muối= m kim loại +m gốc axit
6,545 =m kim loại + 0,065.2.36,5
=>m kim loại =1,93g

Chọn đáp án A
Mg + 2HCl → MgCl2 + H2↑ || Zn + 2HCl → ZnCl2 +H2↑.
nH2↑ = 0,15 mol ⇒ nCl− trong muối = 2nH2 = 0,3 mol.
||→ m = mmuối = mkim loại + mCl− = 5,65 + 0,3 × 35,5 = 16,3 gam. Chọn A.

Vận dụng phương pháp tăng giảm khối lượng.
Theo phương trình ta có:
Cứ 1 mol muối C O 3 2 - → 2 mol Cl- + lmol CO2 lượng muối tăng 71 - 60 = 11 g
Theo đề số mol CO2 thoát ra là 0,03 thì khối lượng muối tăng 11.0,03 = 0,33 g
Vậy m muối clorua = 14 + 0,33 = 14,33 g.
Đáp án B


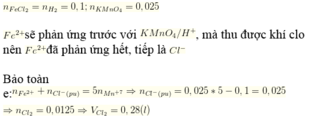

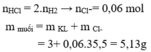
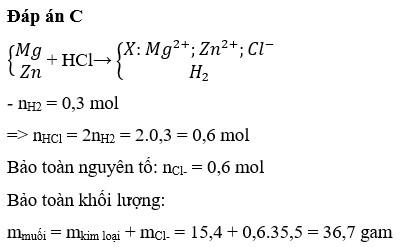
Đáp án C