Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tăng giảm khối lượng ta có mO/MgO = 28 – 20 = 8 gam.
Bảo toàn nguyên tố Mg ta có nMg = nMgO = 8 ÷ 16 = 0,5 mol.
⇒ nNO2 = 2nMg = 1 mol Û VNO2 = 22,4 lít
Đáp án D

Đáp án B
Ta nhận thấy mE < mX => KL chưa phản ứng hết; AgNO3 và Cu(NO3)2 hết
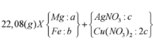
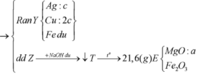
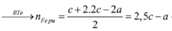
![]()

Đáp án C
Có mhỗn hợp rắn < mFe => Chứng tỏ X chưa tan hết.
=> Fe bị oxi hóa lên Fe(II)
Đặt số mol Fe phản ứng và Fe dư lần lượt là x, y.
24 . n Mg + 56 . m Fe = 7 , 36 g → BTe 2 . n Mg + 2 x + 3 y = 2 . n SO 2 = 2 . 5 , 04 22 , 4 = 0 , 45 mol m MgO + m Fe 2 O 3 = 40 . n Mg + 160 . x 2 = 7 , 2 g ⇒ n Mg = 0 , 12 mol x = 0 , 03 y = 0 , 05
⇒ % m Fe ( X ) = 56 . ( x + y ) 7 , 36 . 100 % = 60 , 87 %

Đáp án D
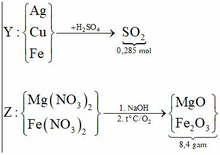
(Mg, Fe) + (AgNO3, Cu(NO3)2) => 3 kim loại
=> Chứng tỏ Mg, AgNO3, Cu(NO3)2 phản ứng hết, Fe còn dư; 3 kim loại là Ag, Cu, Fe.
Dung dịch Z chứa Mg(NO3)2 và Fe(NO3)2.
Đặt số mol Mg, Fe phản ứng, Fe dư lần lượt là a, b, c
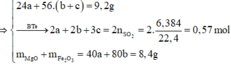
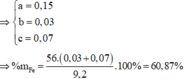


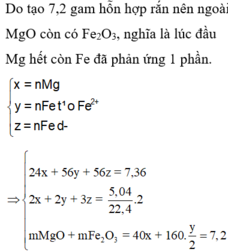
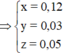
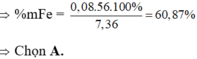
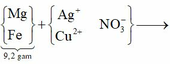

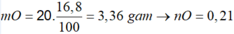
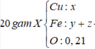
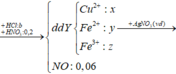
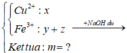
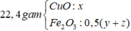
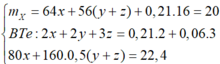
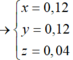
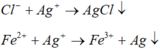
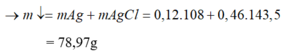

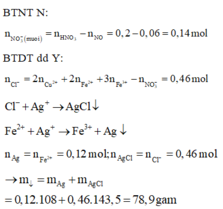
Đáp án C
28g chất rắn gồm MgO và Fe2O3=> mO trong MgO = 28 – 20 = 8g => nMg = mO = 0,5
Bảo toàn ne=> nNO2 = 2nMg = 1 => V = 22,4