Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
\(m_{H_2SO_4}=196.40\%=78,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{78,4}{98}=0,8\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Mol: 0,2 0,6 0,2
Ta có: \(\dfrac{0,2}{1}< \dfrac{0,8}{3}\) ⇒ Fe2O3 hết, H2SO4 dư
mdd sau pứ = 32 + 196 = 228 (g)
\(C\%_{ddFe_2\left(SO_4\right)_3}=\dfrac{0,2.400.100\%}{228}=35,09\%\)
\(C\%_{ddH_2SO_4dư}=\dfrac{\left(0,8-0,6\right).98.100\%}{228}=8,596\%\)

Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Ta lại có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{294}.100\%=20\%\)
=> \(m_{H_2SO_4}=58,8\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
Ta thấy: \(\dfrac{0,2}{1}=\dfrac{0,6}{3}\)
Vậy không có chất dư.
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
Ta có: \(m_{dd_{Al_2\left(SO_4\right)_3}}=294+5,4-\left(\dfrac{3}{2}.0,2.2\right)=298,8\left(g\right)\)
=> \(C_{\%_{Al_2\left(SO_4\right)_3}}=\dfrac{34,2}{298,8}.100\%=11,45\%\)

\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,02 0,02
\(n_{CuSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{CuSO4}=0,02,160=3,2\left(g\right)\)
\(m_{ddspu}=1,6+300=301,6\left(g\right)\)
\(C_{CuSO4}=\dfrac{3,2.100}{301,6}=1,6\)0/0
Chúc bạn học tốt

a) Đặt: nMg=x(mol); nZnO=y(mol)
nH2SO4= 0,2(mol)
PTHH: Mg + H2SO4 -> MgSO4 + H2
x___________x____x_______x(mol)
ZnO + H2SO4 -> ZnSO4 + H2O
y____y______y(mol)
Ta có:
\(\left\{{}\begin{matrix}24x+81y=12,9\\22,4x=4,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
mMg=0,2.24=4,8(g)
%mMg=(4,8/12,9).100=37,209%
=>%mZnO=62,791%
b) nH2SO4=x+y=0,3(mol)
=> \(C\%ddH2SO4=\dfrac{0,3.98}{120}.100=24,5\%\)

thôi thì mình làm cho bn vậy, câu a ko làm dc đâu, làm câu b thôi, làm sao biết dc chất nào dư khi chỉ có số mol 1 chất?
nK2SO3=0.1367(mol)
mddH2SO4=Vdd.D=200.1,04=208(g)
K2SO3+H2SO4-->K2SO4+H2O+SO2
0.1367----0.1367----0.1367---------0.1367 (mol)
mddspu=100+208-0,1367.64=299.2512(g) ; mK2SO4=0,1367.174=23.7858(g)
==>C%=23.7858.100/299.512=7.94%
2)pt bn tự ghi nhé
ta có hệ pt: 56a+27b=11 và a+3b/2=8.96/22.4==>a=0.1, b=0.2
==>%Fe=0.1x56x100/11=50.9%
%Al=100%-50.9%=49.1%
b)nH2SO4= 0.7(mol)==>VddH2SO4=0.7/2=0.35(L)

Bài 4 :
\(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
300ml = 0,3l
\(n_{HCl}=1.0,3=0,3\left(mol\right)\)
1) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,1 0,3 0,1
2) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\)
⇒ MgO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của MgO
\(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{MgCl2}=0,1.95=9,5\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,3-\left(0,1.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=1,14.300=342\left(g\right)\)
\(m_{ddspu}=4+342=346\left(g\right)\)
\(C_{MgCl2}=\dfrac{9,5.100}{346}=2,75\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{346}=1,05\)0/0
Chúc bạn học tốt

Ta có: \(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
PTHH: MgO + 2HCl ---> MgCl2 + H2.
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,1\left(mol\right)\)
=> \(m_{MgCl_2}=0,1.95=9,5\left(g\right)\)
Ta có: \(m_{dd_{MgCl_2}}=4+100=104\left(g\right)\)
=> \(C_{\%_{MgCl_2}}=\dfrac{9,5}{104}.100\%=9,13\%\)

a, \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
b, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\)
\(\Rightarrow m_{MgO}=4,4-2,4=2\left(g\right)\)
c, \(n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{Mg}+n_{MgO}=0,15\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,15.98=14,7\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{14,7}{19,6\%}=75\left(g\right)\)

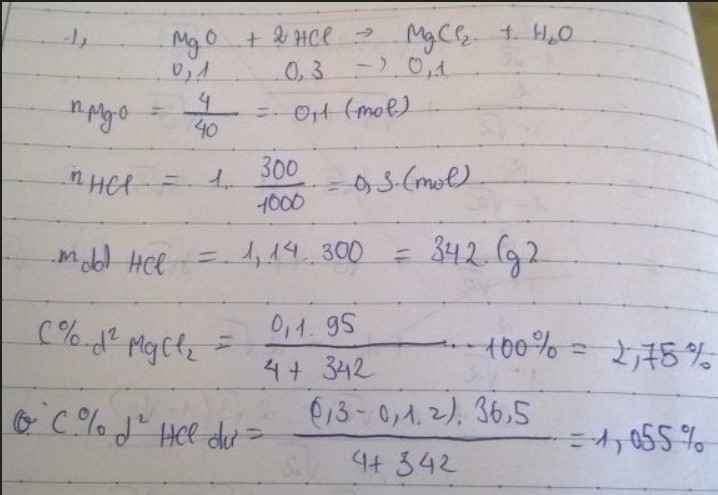
PTHH: \(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{40}{40}=1\left(mol\right)\\n_{H_2SO_4}=\dfrac{300\cdot98\%}{98}=3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{MgSO_4}=1\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{120}{300+40}\cdot100\%\approx35,3\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{2\cdot98}{300+40}\cdot100\%\approx57,65\%\end{matrix}\right.\)