Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mik sửa lại cái dưới bị lỗi latex
\(a.n_{HCl}=0,05.2=0,1\left(mol\right);n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.C_{M_{AlCl_3}}=\dfrac{0,3.2:3}{0,05}=0,4M\\ C_{M_{HCl\left(dư\right)}}=\dfrac{0,1-\left(0,3.6:3\right)}{0,05}=0,8M\)
\(a.n_{HCl}=0,05.2=0,1\left(mol\right)\\ n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.n_{AlCl_3}=n_{Al}=0,02mol\\ C_{M_{AlCl_3}}=\dfrac{0,02}{0,05}=0,4M\\ C_M_{HCl\left(dư\right)}=\dfrac{0,1-\left(0,03.2\right)}{0,05}=0,8M\)

a) nH2=0,0672/22,4=0,03(mol)
2R + 6HCl->2 RCl3 + 3H2
0,02<-.................0,02.<-0,03 (mol)
R=0,54/0,02=27
=> R là Al
b) CMddAlCl3=0,02/0,5=0,04M

\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_R=n_{H2}=0,3\left(mol\right)\Rightarrow M_R=\dfrac{16,8}{0,3}=56\left(Fe\right)\)
Vậy kim loại R là sắt

\(n_{H_2}=\dfrac{10,08}{22,4}=0,45(mol)\\ 2R+6HCl\to 2RCl_3+3H_2\\ \Rightarrow n_{R}=\dfrac{2}{3}n_{H_2}=0,3(mol)\\ \Rightarrow M_{R}=\dfrac{8,1}{0,3}=27(g/mol)\)
Vậy R là Al

Gọi KL là R
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6(mol)\\ a,2R+6HCl\to 2RCl_3+3H_2\\ \Rightarrow n_R=0,4(mol)\\ \Rightarrow M_R=\dfrac{10,8}{0,4}=27(g/mol)(Al)\\ b,n_{HCl}=1,2(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{1,2.36,5}{14,6\%}=300(g)\)

\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
0,15<-0,3<---0,15<----0,15
a. \(M=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
Vậy M là kim loại Fe.
b. \(n_{NaOH}=0,5.1=0,5\left(mol\right)\)
\(HCl+NaOH\rightarrow NaCl+H_2O\)
0,2<-----0,2
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,15----->0,3
\(m_{dd.HCl}=\dfrac{\left(0,3+0,2\right).36,5.100\%}{10\%}=182,5\left(g\right)\)
\(m_{dd.A}=8,4+182,5-0,15.2=190,6\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{127.0,2.100\%}{190,6}=13,33\%\)
\(C\%_{HCl.dư}=\dfrac{0,3.36,5.100\%}{190,6}=5,75\%\)

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
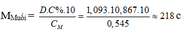
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
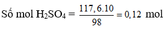
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
a) \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
nHCl = 0,05.2 = 0,1
Có 2.nH2 < nHCl => R phản ứng hết
PTHH: 2R + 6HCl --> 2RCl3 + 3H2
____0,02<-----------------------0,03
=> \(M_R=\dfrac{0,54}{0,02}=27\left(Al\right)\)
b)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
___________0,06<----0,02<---0,03
=> \(\left\{{}\begin{matrix}C_{M\left(HCldư\right)}=\dfrac{0,1-0,06}{0,05}=0,8M\\C_{M\left(AlCl_3\right)}=\dfrac{0,02}{0,05}=0,4M\end{matrix}\right.\)
Cảm ơn bạn rất nhiều