
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 18:
\(n_{NO}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ \text{Đ}\text{ặt}:n_{Al}=a\left(mol\right);n_{Fe}=b\left(mol\right)\left(a,b>0\right)\\ Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\\ Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,15\\27a+56b=5,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\\ \Rightarrow\%m_{Al}=\dfrac{0,1.27}{5,5}.100\approx49,091\%;\%m_{Fe}\approx50,909\%\\ b,n_{HNO_3}=4.n_{NO}=0,6\left(mol\right)\\ V_{\text{dd}HNO_3}=\dfrac{0,6}{0,3}=2\left(M\right)\)
c) Dung dịch Y là dung dịch nào?

5. a) Tính chất vật lí để thực hiện phương pháp này là do anken không tan trong nước và nhẹ hơn nước
b) PTHH: C2H5OH → C2H4 + H2O (Xúc tác của H2SO4 đặc, nhiệt độ 170 độ C)

Câu 1
a) \(CH_2=CH-CH=CH_2+H_2\underrightarrow{t^o,Ni}CH_3-CH_2-CH=CH_2\)
b) \(CH_2=CH-CH=CH_2+Br_2\rightarrow CH_2Br-CHBr-CH=CH_2\)
c) \(nCH_2=C\left(CH_3\right)-CH=CH_2\underrightarrow{t^o,p,xt}\left(-CH_2-C\left(CH_3\right)=CH-CH_2-\right)_n\)
d) \(CH\equiv C-CH_3+2H_2\underrightarrow{t^o,Ni}CH_3-CH_2-CH_3\)
e) \(CH\equiv C-CH_3+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH-CH_3\)
f) \(CH\equiv CH+2HCl\underrightarrow{t^o,xt}CH_3-CHCl_2\)
g) \(CH\equiv C-CH_3+HOH\underrightarrow{Hg^{2+},H^+}CH_3-CO-CH_3\)
h) \(CH\equiv C-CH_3+AgNO_3+NH_3\underrightarrow{H_2O}CAg\equiv C-CH_3\downarrow+NH_4NO_3\)
Câu 2:
a)
\(CH_3COONa+NaOH\underrightarrow{CaO,t^o}CH_4+Na_2CO_3\)
\(2CH_4\underrightarrow{1500^oC,làm.lạnh.nhanh}CH\equiv CH+3H_2\)
\(CH\equiv CH+HCl\underrightarrow{t^o,xt}CH_2=CHCl\)
\(nCH_2=CHCl\underrightarrow{t^o,p,xt}\left(-CH_2-CHCl-\right)_n\)
b)
CaCO3 --to--> CaO + CO2
CaO + 3C --to--> CaC2 + CO
CaC2 + 2H2O --> \(CH\equiv CH+Ca\left(OH\right)_2\)
\(2CH\equiv CH\underrightarrow{đime.hóa}CH\equiv C-CH=CH_2\)
\(CH\equiv C-CH=CH_2+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH-CH=CH_2\)
\(nCH_2=CH-CH=CH_2\underrightarrow{t^o,p,xt}\left(-CH_2-CH=CH-CH_2\right)_n\)
c) X: CH4, Y: C2H4
(1) \(CH_3-CH_2-CH_3\underrightarrow{t^o,xt}CH_4+CH_2=CH_2\)
(2) \(2CH_4\underrightarrow{1500^oC,làm.lạnh.nhanh}CH\equiv CH+3H_2\)
(3) \(CH\equiv CH+2H_2\underrightarrow{t^o,Ni}CH_3-CH_3\)
(4) \(CH\equiv CH+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH_2\)
(5) \(CH_2=CH_2+H_2O\underrightarrow{H^+,t^o}CH_3-CH_2OH\)
(6) \(CH_3-CH_2OH\underrightarrow{H_2SO_4,170^oC}CH_2=CH_2\)

Câu 2.
a) Cho 2 khí lội qua dung dịch AgNO3/NH3
+Khí nào phản ứng có kết tủa : propin
CH≡C–CH3 + AgNO3 + NH3 → AgC≡C–CH3 + NH4NO3
+Khí còn lại không có hiện tượng : propen
b) Trích mỗi chất 1 ít làm mẫu thử
- Cho dung dịch Cu(OH)2 vào từng mẫu thử
+ Mẫu thử nào phản ứng, xuất hiện dung dịch màu xanh lam là Glyxerol
Cu(OH)2 + 2C3H5(OH)3 ⟶ 2H2O + [C3H5(OH)2O]2Cu
+ 2 mẫu thử còn lại không phản ứng là ancol etylic và phenol
- Cho dung dịch Brom vào 2 mẫu thử không phản ứng với Cu(OH)2
+ Mẫu thử nào xuất hiện kết tủa : C6H5OH
3Br2 + C6H5OH ⟶ C6H2Br3OH + 3HBr
+ Còn lại không phản ứng là C2H5OH

22)
C3H7OH + Na → C3H7ONa + 1/2H2
nC3H7OH = 6:60 = 0,1 mol
=> nC3H7ONa = 0,1 mol và nH2 = 0,05 mol
<=> mC3H7ONa = 0,1.82= 8,2 gam, VH2 = 0,05.22,4 = 1,12 lít
23)
C6H5OH + 3Br2 → C6H2(OH)Br3↓ + 3HBr
nC6H2(OH)Br3 = 33,1:331 = 0,1 mol
=> nC6H5OH = 0,1 mol
<=> mC6H5OH = 0,1.94 = 9,4 gam
24)
C2H5CHO + 2AgNO3 + 3NH3 + H2O → C2H5COONH4 + 2Ag + 2NH4NO3
nC2H5CHO = 5,8:58 = 0,1 mol
=> nAg = 0,2 mol
<=> mAg = 0,2.108 = 21,6 gam
25)
CH3COOH + NaOH → CH3COONa + H2O
nCH3COOH = \(\dfrac{50.6\%}{60}\) = 0,05 mol
=> nNaOH = 0,05 mol
<=> VNaOH = 0,05:2 = 0,025 lít = 25ml

Câu 24 :
$n_{OH^-\ pư} = n_{H^+} = 0,1.10^{-1} = 0,01(mol)$
$n_{OH^-\ dư} = 0,2.(10^{-14} : 10^{-12}) = 0,002(mol)$
$\Rightarrow n_{OH^-} = 0,01 + 0,002 = 0,012(mol)$
$\Rightarrow a = \dfrac{0,012}{0,1} = 0,12M$
Đáp án D











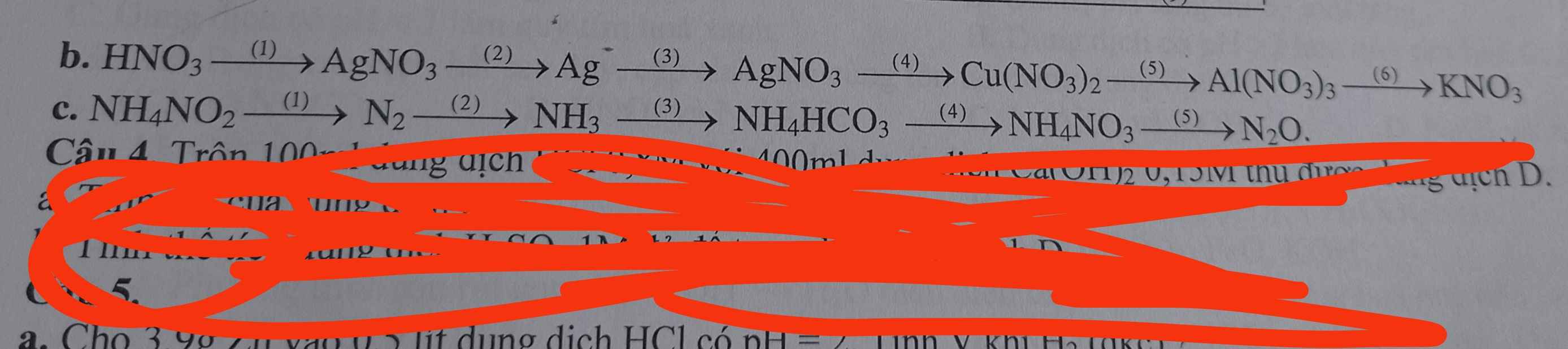


Câu 4 :
\(n_{H^+}=0.2\cdot0.5\cdot2+0.2\cdot0.25=0.25\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.25......0.25\)
\(n_{OH^-\left(dư\right)}=0.001V-0.25\left(mol\right)\)
\(C_{M_{OH^-\left(dư\right)}}=\dfrac{0.001V-0.25}{0.2+0.001V}\left(M\right)\)
\(pH=13\)
\(\Rightarrow log\left[OH^-\right]=13-14=-1\)
\(\Rightarrow log\left(\dfrac{0.001V-0.25}{0.2+0.001V}\right)=-1\)
\(\Rightarrow V=300\)
Câu 5 :
\(pH=1\Rightarrow\left[H^+\right]=0.1\)
\(pH=13\Rightarrow\left[OH^-\right]=0.1\)
\(n_{H^+}=0.1V_1\left(mol\right)\)
\(n_{OH^-}=0.1V_2\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.1V_1...0.1V_1\)
\(n_{OH^-\left(dư\right)}=0.1V_2-0.1V_1\left(mol\right)\)
\(\left[OH^-\right]\left(dư\right)=\dfrac{0.1V_2-0.1V_1}{V_1+V_2}\left(M\right)\)
\(pH=14+log\left[OH^-\right]=12\)
\(\Rightarrow\left[OH^-\right]=0.01\)
\(\Rightarrow\dfrac{0.1V_2-0.1V_1}{V_1+V_2}=0.01\)
\(\Leftrightarrow V_2-V_1-0.1V_1-0.1V_2=0\)
\(\Leftrightarrow0.9V_2-1.1V_1=0\)
\(\Leftrightarrow\dfrac{V_1}{V_2}=\dfrac{0.9}{1.1}=\dfrac{9}{11}\)