Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi nAl=x mol và nFe2O3 = y mol
Fe2O3 + 2Al → Al2O3 + 2Fe
Đầu(mol) y x
Do chất rắn sau +NaOH tạo khí nên dư Al
=> nH2=1,5nAl => 0,06= x-a mX= 160y + 27x = 21,67
m rắn không tan = mFe2O3 + mFe = 160(y – ½ a) + 56a=12,4
Giải hệ : x=0,21mol ; y=0,1mol ; a =0,15mol.
Tính hiệu suất theo Fe2O3 => %H= (0,075/0,1) .100%= 75%
=>D

Đáp án B.
2 A l + F e 2 O 3 → t o A l 2 O 3 + 2 F e
· Phần 1 + NaOH → 0,75 mol H2
=> Al dư, Fe2O3 phản ứng hết.
n A l = 2 3 n H 2 = 0 , 5 m o l
· Đặt số mol Fe, A l 2 O 3 trong phần 1 lần lượt là 2x, x.
Giả sử phần 2 có khối lượng gấp k lần phần 1.
=> (27.0,5 + 56.2x + 102x).(k – 1)=134 (1)
· Phần 2:
n H 2 = n F e + 3 2 n A l ⇒ k . 2 x + 3 2 k . 0 , 5 = 84 22 , 4 = 3 , 75 m o l ( 2 )
· Từ (1) và (2) suy ra:
x = 60 107 ; k = 2 x = 0 , 25 ; k = 3 ⇒ m F e = 56 . 2 x . ( k + 1 ) = 188 , 4 g 112 g
Kết hợp đáp án suy ra
m
F
e
=
112
g
.
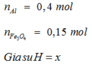
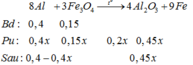
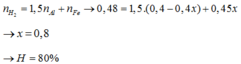


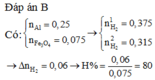
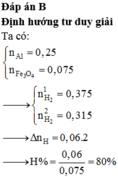
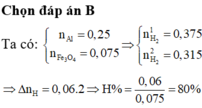
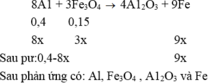
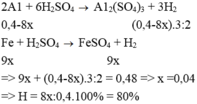

Đáp án B
nAl = 10,8: 27 = 0,4 mol ; nFe3O4 = 34,8: 232 = 0,15 mol
Ta thấy: 0,4/8 = 0,15/3 nên hiệu suất có thể tính theo Al hoặc Fe3O4
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
Mol x → 1,125x => nAl dư = (0,4 –x) mol
Khi chất rắn sau phản ứng + HCl thì:
Al + 3HCl → AlCl3 + 1,5H2
Mol (0,4 – x) → 1,5(0,4 – x)
Fe + 2HCl → FeCl2 + H2
Mol 1,125x → 1,125x
=> nH2 = 1,5(0,4 – x) + 1,125x = 10,416: 22,4 = 0,465 mol
=> x = 0,36 mol
Tính H theo Al => H% = nPứ / nbđ = 0,36: 0,4 = 90%