Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Nhỏ từ từ H2SO4 vào dd X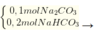 ddY + 0,2 mol CO2.
ddY + 0,2 mol CO2.
ddY + Ba(OH)2 dư → m↓ = ? gam
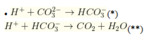
Theo (*) ![]()
Theo (**) ![]()
Dung dịch X gồm H C O 3 - dư 0,1 mol; H2SO4 0,15 mol.
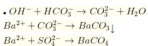
nBaCO3 = 0,1 mol; nBaSO4 = 0,15 mol
→ m↓ = mBaCO3 + mBaSO4 = 0,1 × 197 + 0,15 × 233 = 54,65 gam → Đáp án đúng là đáp án A

n H + = 2 n H 2 S O 4 = 0 , 15 . 2 = 0 , 3 ; n S O 4 2 - = 0 , 15 v à n C O 3 2 - = 0 , 1 ; n H C O 3 - = 0 , 3
Xác định tỉ lệ số mol của C O 3 2 - v à H C O 3 - và trong dung dịch ta có:
n N a 2 C O 3 n N a H C O 3 = 0 , 1 0 , 3 = 1 3
So sánh số mol: Ta có: ( 2 n C O 3 2 - + n H C O 3 2 - ) = 0 , 5 > n H + = 0 , 3 ⇒ H + h ế t
Khi cho từ từ A vào B nên C O 3 2 - và H C O 3 - sẽ đồng thời phản ứng với axit.
Vì vậy giả sử nếu C O 3 2 - phản ứng hết x mol thì H C O 3 - sẽ phản ứng 1 lượng đúng bằng tỉ lệ mol trong dung dịch của 2 chất là 3x mol.
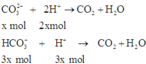
Do H+ hết nên tính theo H+ ta có: 5x = 0,3 ⇒ x = 0,6
⇒ Trong X chứa anion: H C O 3 - (0,3 – 3.0,6 = 0,12 mol), C O 3 2 - (0,1 – 0,06 = 0,04 mol) và S O 4 2 - (0,15 mol)
Khi cho Ba(OH)2 dư vào ta có các phản ứng:
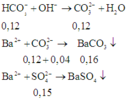
Vậy khối lượng kết tủa thu được là:
![]()

Nhận thấy kết lớn nhất khi BaSO4: 0,03 mol, Al(OH)3: 0,04 mol
Vậy nOH-= 3×nAl3+ = 0, 12 mol
nK = 0,12 - 2×nBa(OH)2- nNaOH = 0,03 mol → mK = 1,17
Đáp án B

Đáp án C
Quy quá trình thành: CO2 + 0,2 mol Ba(OH)2 + Ca(OH)2 dư → 49,4g ↓
⇒ nCaCO3 = (49,4 - 0,2 × 197) ÷ 100 = 0,1 mol. Bảo toàn nguyên tố Cacbon:
nCO2 = nBaCO3 + nCaCO3 = 0,2 + 0,1 = 0,3 mol ⇒ chọn C.

Nhận thấy kết lớn nhất khi BaSO4: 0,03 mol, Al(OH)3: 0,04 mol
Vậy nOH-= 3×nAl3+ = 0, 12 mol
nNa = 0,12 - 2×nBa(OH)2- nNaOH = 0,03 mol → mNa = 0,69.
Đáp án D

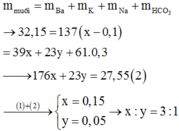

Bảo toàn điện tích :
$n_{CO_3^{2-}} + n_{SO_3^{2-}} + n_{SO_4^{2-}} = \dfrac{0,4 - 0,2}{2} = 0,1$
$HCO_3^- + OH^- \to CO_3^{2-} + H_2O$
Suy ra:
$n_{CO_3^{2-}} + n_{SO_3^{2-}} + n_{SO_4^{2-}} = 0,1 + + n_{HCO_3^-} = 0,1 + 0,2 = 0,3$
$\Rightarrow n_{Ba(OH)_2} = n_{Ba^{2+}} = n_{CO_3^{2-}} + n_{SO_3^{2-}} + n_{SO_4^{2-}} = 0,3(mol)$