Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Ta có: nHCl= 0,45 mol; n C O 2 = 5,6/22,4= 0,25 mol.
Giả sử ban đầu có x mol NaHCO3
CO32- + H+ → HCO3- (1)
HCO3-+ H+ → CO2+ H2O (2)
0,25 0,25 ←0,25
Theo PT (2): n H C O 3 - = n H + = n C O 2 = 0,25 mol
→ n H + PT1 = 0,45- 0,25 = 0,2 mol
→ n C O 3 2 - PT1 = n H + = n H C O 3 - PT1 = 0,2 mol
→ n N a 2 C O 3 = n C O 3 2 - PT1= 0,2 mol
→ C M N a 2 C O 3 = 0,2/ 0,5 = 0,4M
Dung dịch Y chứa Na+, HCO3- dư: x+0,2- 0,25= x- 0,05 mol
HCO3-+ OH- → CO32-+ H2O
Ba2++ CO32- → BaCO3
Ta thấy: n H C O 3 - = n C O 3 2 - = n B a C O 3 = 19,7/197 = 0,1 mol
→ x- 0,05 = 0,1 → x = 0,15 mol
→ C M N a H C O 3 = 0,15/ 0,5 = 0,3M

Đáp án D
Gọi n N a 2 C O 3 = x ; n N a H C O 3 = x và n B a ( H C O 3 ) 2 = y
Khi hòa tan hỗn hợp vào nước có phản ứng:
![]()
Khi đó trong dung dịch X có NaHCO3, Ba(HCO3)2 dư hoặc Na2CO3.
Dù thành phần của dung dịch X như thế nào thì toàn bộ số mol trong hỗn hợp ban đầu và trong dung dịch X là như nhau.
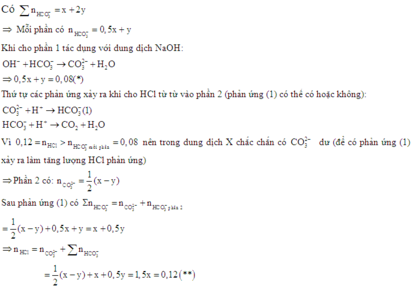
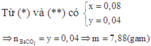

Gọi thể tích của dung dịch HCl là V(lít)
Các phản ứng
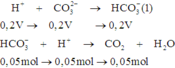
Sau phản ứng cho nước vôi trong dư vào dung dịch Y thì được kết tủa
Trong dung dịch Y còn chứa anion H C O 3 - ⇒ H+ phản ứng hết.
Sau (1), (2) có n H C O 3 - còn lại = 0,2V – 0,05 + 0,1 = 0,2V + 0,05
Khi cho nước vôi trong vào dung dịch Y ta có phản ứng sau:
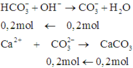
Do đó, ta có 0,2V + 0,05 = 0,2 mol ⇒ V = 0,75
Tổng số mol HCl là: 0,2V + 0,05 = 0,2 . 0,75 + 0,05 = 0,2 mol
Nồng độ của HCl: C M = n v = 0 , 2 0 , 2 = 1 M
Đáp án C.

NaOH + HCl → NaCl + H2O
0,1...........0,1.................................(mol)
Na2CO3 + HCl → NaCl + NaHCO3
0,15............0,15.....................0,15..........(mol)
NaHCO3 + HCl → NaCl + CO2 + H2O
0,05............0,05...................0,05.............(mol)
=> a = 0,05
Bảo toàn nguyên tố C :
n BaCO3 = n NaHCO3 dư = 0,15 - 0,05 = 0,1(mol)
=> m = 0,1.197 = 19,7(gam)

KOH + HCl → KCl + H2O
0,1........0,1.......0,1...................(mol)
Na2CO3 + HCl → NaHCO3 + NaCl
0,2.............0,2.............0,2............................(mol)
NaHCO3 + HCl → NaCl + CO2 + H2O
0,1.............0,1....................0,1..................(mol)
Suy ra : a = 0,2
Sau phản ứng : n NaHCO3 = 0,2 - 0,1 = 0,1(mol)
Bảo toàn nguyên tố C :
n CaCO3 = n NaHCO3 = 0,1(mol)
=> m = 0,1.100 = 10(gam)
anh ơi giải thích giúp e cái phương trình thứ hai được không ạ tại sao lại ra 0,2 ạ, trong khi đó số mol hcl dư là 0,4 - 0,1 =0,3

n CaCO 3 = 0 , 5 ⇒ n CO 3 2 - = 0 , 5
n H 2 SO 4 = 0 , 3 . 0 , 5 = 0 , 15 ⇒ n H + = 0 , 3 ; n SO 4 2 - = 0 , 15
Ta có: n CO 3 2 - > n H + => Chỉ xảy ra phản ứng: H + + CO 3 2 - → HCO 3 - và CO 3 2 - còn dư
Vậy dung dịch Y chứa 6 muối chỉ có thể là
Na2CO3; K2CO3; KHCO3; NaHCO3; Na2SO4; K2SO4
Trong Y chứa các anion: CO 3 2 - ( a mol ) ; HCO 3 - ( b mol ) ; SO 4 2 - ( 0 , 15 mol )
Khi thêm Ba(OH)2 dư vào dung dịch Y ta có các phản ứng:

Ta có a + b = n CO 3 2 - = 0 , 5 ⇒ m = 0 , 5 . 197 + 0 , 15 . 233 = 133 , 45 gam
Đáp án C


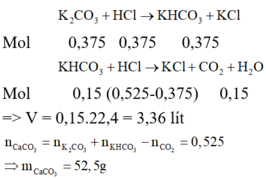
Đáp án B
Như vậy, trong X chỉ có 0,2 mol CO3 2-
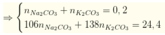
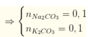
=> Đáp án B