Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thuần đốt cháy :
⇒ nhìn hỗn hợp hiđrocacbon gồm a mol C + b mol H2.
Đốt cháy 1,84 gam hỗn hợp + O2 a mol CO2 + b mol H2O.
Ta có :
Ca(OH)2 dùng dư :
Δmdung dịch giảm = mCaCO3↓ – ∑(mCO2 + mH2O)
→Ta có: 100a – (44a + 18b) = 4,76
=>56a – 18b = 4,76. (1)
Lại có :
12a + 2b = mhỗn hợp = 1,84 (2)
Từ 1, 2=> a = 0,13; b = 0,14.
→ m gam kết tủa là 0,13 mol CaCO3 → m = 13,0 gam.

Nhận thấy các chất trong hỗn hợp đều có dạng Cm(H2O)n nên có thể quy về C và H2O.
Đốt cháy hỗn hợp thu được sản phẩm dẫn vào Ba(OH)2 dư thu được kết tủa là BaCO3 0,47 mol nên C 0,47 mol.
Khối lượng dung dịch giảm 65,07 gam.
\(\rightarrow mH_2O=92,59-65,07-0,47.44=6,84\left(g\right)\)
\(\rightarrow m=6,84+0,47.12=12,48\left(g\right)\)
=> chọn D
nCO2 = nBaCO3 = 0,47 mol => nC = 0,47 mol
m dung dịch giảm = mBaCO3 – mCO2 – mH2O
=> 65,07 = 92,59 – 0,47.44 – mH2O
=> mH2O = 6,84 gam => nH2O = 0,38 mol => nH = 0,76 mol
CTPT các chất lần lượt là: C3H4O2, C2H4O2, C6H10O5
=> nO = n\(\dfrac{H}{2}\) = 0,38 mol
->m = mC + mH + mO = 0,47.12 + 0,76 + 0,38.16 = 12,48 gam

Đáp án C.
nBa(OH)2= 0,1.2 = 0,2 (mol); nBaSO3 = 0,1 (mol)
nBaSO3 = 2 nBa(OH)2 - nSO2 ⇒ nSO2 = 2.0,2 – 0,1 = 0,3 (mol)
FeS2 → 2SO2 (Bảo toàn S)
0,15 0,3 (mol)
⇒ mFeS2 = 0,15.(56+32.2) = 18 (g)


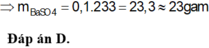

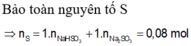
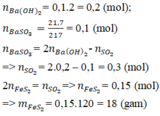
Ta có: m dd tăng = mCO2+H2O - mCaCO3 => mCO2+H2O = 25,4 + 10 = 35,4 gam
TH1: Ca(OH)2 dư, CaCO3 chưa bị hòa tan
CO2 + Ca(OH)2 → CaCO3, Ca(OH)2 dư, H2O
=> nCO2 = nCaCO3 = 0,1 mol => mH2O = 35,4 - 0,1.44 = 31 gam
=> nH2O = 1,722 mol > nCO2 (loại)
TH2: CaCO3 bị hòa tan một phần
CO2 + Ca(OH)2 → CaCO3, Ca(HCO3)2, H2O
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 - nCaCO3 = 0,35 - 0,1 = 0,25 mol
BTNT "C": nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,1 + 2.0,25 = 0,6 mol
=> mH2O = 35,4 - 0,6.44 = 9 gam => nH2O = 0,5 mol
=> n axit = nCO2 - nH2O = 0,6 - 0,5 = 0,1 mol
=> nO(axit) = 2naxit = 0,2 mol
=> m = m axit = mC + mH + mO = 0,6.12 + 0,5.2 + 0,2.16 = 11,4 gam
thanh kiêu