Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
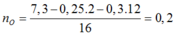
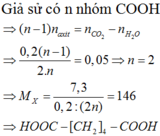
Khối lượng este thu được: m = 0,2.(29 + 44 + 14.4 + 44 + 29) = 40,4
=> Đáp án D

$n_C = n_{CO_2} = 0,135(mol)$
$n_H = 2n_{H_2O} = 0,18(mol)$
$\Rightarrow n_O = \dfrac{4,68 - 0,135.12 - 0,18}{16} = 0,18(mol)$
Ta có :
$n_C : n_H : n_O = 0,135 : 0,18 : 0,18 = 3 : 4 : 4$
Vậy axit là $HOOC-CH_2-COOH$
$CH_2(COOH)_2 + 2CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_2(COOCH_3)_2 + 2H_2O$
$n_{este} = n_{axit\ pư} = 0,25.60\% = 0,15(mol)$
$m_{este} = 0,15.132 = 19,8(gam)$

Các axit và ancol đều no nên X là este no.
3nX phản ứng = nCO2 - nH2O => X có k = 4 (dựa vào công thức: nX = (nCO2-nH2O)/(k-1))
X tạo bởi 2 axit và 1 ancol nên X có 3 nhóm COO và 1 vòng
Giả sử X có công thức: B(COO)2(ACOO)R (a mol)
=> M gồm ACOOH (a mol); B(COOH)2 (a mol), R(OH)3 (a mol)
Quy đổi hỗn hợp M thành HCOOH (a); (COOH)2 (a); C3H5(OH)3 (a) và CH2 (b)
+ nH2O = a + a + 4a + b = 0,6
Lượng O2 dùng để đốt X cũng như đốt M nên:
+ nO2 = 0,5a + 0,5a + 3,5a + 1,5b = 0,5625
Giải hệ trên thu được a = 0,075 và b = 0,15
Do b = 2a nên X là HCOO(COO)2C3H5.2CH2
=> X là C8H10O6
Đáp án cần chọn là: D

Đáp án A
nC2H5OH = 0,1 mol; nCH3COOH = 0,1 mol.
CH3COOH + C2H5OH <=> CH3COOC2H5 + H2O
mCH3COOC2H5 = 0,1 × 88 × 80/100 = 7,04 gam → Đáp án A.

Đáp án A
· Thí nghiệm 1: Đốt cháy hoàn toàn a mol T thu được a mol H2O
Þ 2 axit có công thức HCOOH và HOOC – COOH


Đáp án A
Dễ dàng tìm được
X
:
C
4
H
6
O
2
mặt khác X được tạo ra từ phản ứng este hóa giữa ancol Y và axit hữu cơ Z=> X có 2 CTCT:
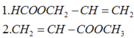

Chọn A gồm (1), (2), (3).
(4) sai vì este đa chức cho nCO2 > nH2O.
(5) sai vì số nguyên tử C chẵn nhưng phải từ 12 đến 24.
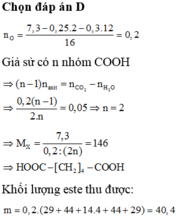
Đáp án D
Gọi công thức của axit là CnH2n+2-2aO2a
=> axit là C6H10O4
=>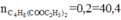
Đáp án D