Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Các quá trình có thể xảy ra ở 2 điện cực:
+) Catot: Cu2+ + 2e → Cu
2H2O + 2e → 2OH- + H2
+) Anot: 2Cl- → Cl2 + 2e
2H2O → 4H+ + O2 + 4e
- Khi điện phân trong t giây:
nkhí Anot = 2,464: 22,4 = 0,11 mol
nCl2 = 0,5nCl- = 0,1 mol < 0,11 => Nước đã bị điện phân ở Anot
=> nO2 = nkhí anot – nCl2 = 0,11 – 0,1 = 0,01 mol
=> ne trao đổi = 2nCl2 + 4nO2 = 2.0,1 + 4.0,01 = 0,24 mol
- Khi điện phân trong 2t giây:
=> Số mol electron trao đổi sẽ gấp đôi: ne trao đổi = 2.0,24 = 0,48 mol
+) Tại Anot: nCl2 = 0,1 mol
Có: ne = 2nCl2 + 4nO2 => nO2 = ¼ (0,48 – 2.0,1) = 0,07 mol
=> nkhí Anot = nCl2 + nO2 = 0,1 + 0,07 = 0,17 mol
nkhí = 5,824: 22,4 = 0,26 mol > 0,17 => Nước bị điện phân ở Catot
=> nH2(Catot) = 0,26 – 0,17 = 0,09 mol
- Bảo toàn e: ne trao đổi = 2nCu2+ + 2nH2 = 4nO2 + 2nCl2
=> nCu2+ = ½ (4.0,07 + 2.0,1 – 2.0,09) = 0,15 mol
=> m = mCuSO4 = 160.0,15 = 24g








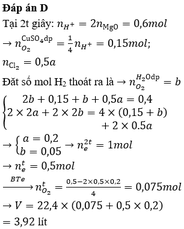


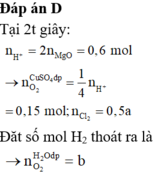

Chọn C
Ở anot xảy ra sự oxi hóa nước: 2H2O → 4H+ + O2 + 4e
nO2 = 0,01 ⇒ ne = 0,04
Mà ne = I.t/96500 ⇒ t = 0,04.96500/10 = 386 giây = 6 phút 26 giây