Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) Để trung hòa HCl, số mol HCl phải bằng số mol NaOH. Vì vậy, ta có:
n(HCl) = n(NaOH)
x * 10 = 0,5 * 50
x = (0,5 * 50) / 10
x = 2,5 triệu
Vậy, nồng độ của dung dịch HCl là 2.5 M.
2) Ta có:
n(HCl) = n(NaOH)
n(HCl) = 0,1 * 20/10
Vậy, nồng độ của dung dịch HCl là 0.2 M.
\(1)n_{NaOH}=0,05.0,5=0,025mol\\ NaOH+HCl\rightarrow NaCl+H_2O\\ \Rightarrow n_{NaOH}=n_{HCl}=0,025mol\)
\(C_M\) \(_{HCl}=\dfrac{0,025}{0,01}=2,5M\)
\(2)n_{NaOH}=0,1.0,02=0,002mol\\ HCl+NaOH\rightarrow NaCl+H_2O\\ n_{NaOH}=n_{HCl}=0,002mol\)
\(C_M\) \(_{HCl}=\dfrac{0,002}{0,01}=0,2M\)

Đáp án A
Thí nghiệm 1 có nOH-= nH+
Nên 30.2= 20.C1+ 20.C2+ 30.1
Thí nghiệm 2 có nOH-= nH+
Nên 10.C1+ 20.C2 = 1.20
Suy ra C1 = 1,0 và C2 = 0,5

Đáp án A
nOH-= nH+ nên 0,02.a+ 0,02.b = 0,3.0,1
nCl-= nAgCl = 0,02 mol = 0,02a suy ra a = 1M suy ra b = 0,5

Đáp án C
nH+ = 0,01.1 + 2.0,01.0,5 = 0,02
nNaOH = nOH- = nH+ = 0,02 ⇒ VNaOH= 0,02l = 20ml.

\(n_{OH^-}=n_{NaOH}=0,3.1,5=0,45\left(mol\right)\\ n_{H^+}=n_{HCl}+2n_{H_2SO_4}=0,2x+0,5.0,2.2=0,2x+0,2\left(mol\right)\)
PT ion rút gọn: \(H^++OH^-\rightarrow H_2O\)
0,45<---0,45
\(\Rightarrow0,2x+0,2=0,45\Leftrightarrow x=1,25M\)
Ta có: \(V_{dd}=0,3+0,2=0,5\left(l\right)\) và \(\left\{{}\begin{matrix}n_{Na^+}=0,45\left(mol\right)\\n_{Cl^-}=0,2.1,25=0,25\left(mol\right)\\n_{SO_4^{2-}}=0,2.0,5=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{Na^+}=\dfrac{0,45}{0,5}=0,9M\\C_{Cl^-}=\dfrac{0,25}{0,5}=0,5M\\C_{SO_4^{2-}}=\dfrac{0,1}{0,5}=0,2M\end{matrix}\right.\)

\(NaOH+HCl \to NaCl+H_2O\\ n_{NaOH}=0,06(mol)\\ \to n_{HCl}=0,06(mol)\\ V_{HCl}=\frac{0,06}{0,6}=0,1(l)=100(ml)\)
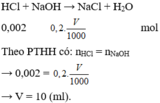
HCl + NaOH → NaCl + H2O
\(n_{HCl}=0,02\times0,1=0,002\left(mol\right)\)
Theo pT: \(n_{NaOH}=n_{HCl}=0,002\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\frac{0,002}{0,01}=0,2\left(M\right)\)
Vậy \(x=0,2\left(M\right)\)
nH+ = 0.002 mol
nOH- = 0.01x mol
H+ + OH- => H2O
0.002_0.002
<=> 0.01x = 0.002
<=> x = 0.2