Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nếu b ≥ 2a thì chắc chắn CO2 sinh ra sẽ như nhau, nhưng đề cho CO2 khác nhau → b < 2a hay a > 0,5b
→ Loại C, D
Thí nghiệm 1: Cho H+ vào CO32-
H+ + CO32- → HCO3-
a a a
H+ + HCO3- → CO2 + H2O
(b – a) → b – a
Thí nghiệm 2: CO32- vào H+
2H+ + CO32- → CO2 + H2O
b → 0,5b
Ta có 0,5b = 2(b – a) → 2a = 1,5b → a = 0,75b
Đáp án A

Đáp án B
TN1: nCO2 = 3,36/22,4 = 0,15 (mol);
+ Cho từ từ HCl vào dd Y sẽ xảy ra phản ứng theo thứ tự:
H+ + CO32-→ HCO3-
H+ + HCO3- → CO2 ↑+ H2O
Áp dụng công thức nhanh => nCO2 = nH+ - nCO32-
=> a – c = 0,15 (1)
TN2: nCO2 = 10,08/ 22,4 = 0,45 (mol)
+ Cho từ từ dd Y vào HCl thì xảy ra đồng thời
HCO3- + H+ → CO2 + H2O
2x → 2x → 2x (mol)
CO32- + 2H+ → CO2 + H2O
x →2x → x (mol)
Vì => phản ứng cũng xảy ra theo tỉ lệ mol như này.
Gọi nCO32- = x thì nHCO3 = 2x
=> nCO2 = 3x = 0,45 (mol) => x = 0,15 (mol)
∑nH+ = 4x = 4. 0,15 = 0,6 (mol) = a
Từ (1) => c = 0,45 (mol)
=> a + b + c = 0,15 + 0,9 + 0,45 = 1,5

Đáp án B
Ta có: n C O 2 = 0,15 mol; n C O 2 (phần 1)= 0,09 mol ; n B a C O 3 = 0,15 mol
Giả sử xảy ra các phản ứng:
CO2+ NaOH→ Na2CO3+ H2O
CO2+ Na2CO3+H2O → 2 NaHCO3
Dung dịch X chứa z mol NaHCO3 và t mol Na2CO3
Xét phần 1 ta có: giả sử có x mol NaHCO3 và y mol Na2CO3 phản ứng
NaHCO3+ HCl → NaCl + CO2+ H2O
Na2CO3+ 2HCl → 2NaCl + CO2+ H2O
Ta có: nHCl = x+2y = 0,12 mol;
n C O 2 = x+y = 0,09 mol
→x = 0,06 và y = 0,03
→ z t = x y = 0 , 06 0 , 03 = 2 → z = 2 t ( * 1 )
Xét phần 2 :
HCO3- + OH- → CO32-+ H2O
0,5z 0,5z
CO32- + Ba2+ → BaCO3 ↓
(0,5z+0,5t)→ (0,5z+0,5t)
→ n B a C O 3 = 0,5z+ 0,5t = 0,15 (*2)
Từ (*1) và (*2) ta có: z = 0,2 mol; t = 0,1 mol
→Dung dịch X chứa 0,2 mol NaHCO3 và 0,1 mol Na2CO3
Quay lại 2 phản ứng đầu :
CO2+ 2NaOH→ Na2CO3+ H2O (1)
0,05→ 0,1 0,05
CO2+ Na2CO3+H2O → 2 NaHCO3 (2)
0,1 0,1 ← 0,2 mol
Ta có: n C O 2 PT 1 = n C O 2 - n C O 2 PT 2 = 0,15- 0,1 = 0,05 mol
Theo PT (1) : nNaOH = a = 0,1 mol
Số mol Na2CO3 còn sau phản ứng (2) là:
b+ 0,05- 0,1 = 0,1→ b = 0,15
Do đó a b = 0 , 1 0 , 15 = 2 3

Đáp án A
Vì thể tích CO2 thu được ở hai lần thí nghiệm khác nhau nên cả hai trường hợp HCl đều hết, chất phản ứng còn lại dư vì nếu ở cả hai trường hợp có các chất đều phản ứng vừa đủ hoặc HCl dư thì lượng CO2 thu được như nhau (bảo toàn nguyên tố C).
Khi cho từ từ từng giọt dung dịch HCl vào dung dịch Na2CO3 có thứ tự các phản ứng xảy ra như sau:
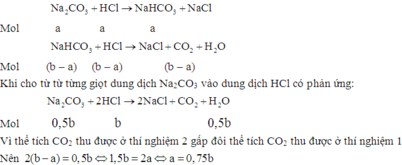


Đáp án A
C1
TH1 : NaHCO3 pư trước
NaHCO3+ HCl →NaCl+H2O+CO2
0.1 0.1 0.1
=>nHCl còn lại = 0.2-0.1=0.1 mol
Na2CO3 + 2 HCl → 2NaCl + H2O + CO2 ( 2 )
0.15 0.1 → 0.05
n CO2 thu đc= 0.1+0.05=0.15mol
VCO2= 0,15 . 22,4= 3.36l
TH2 : Na2CO3 pư trước
Na2CO3 + 2 HCl → 2NaCl + H2O + CO2
0.15 0.2 0.1
sau pư dư 0.05 mol Na2CO3 và còn 0.1 mol NaHCO3 chưa pư
nCO2 thu đc = 0.1 mol
=> V CO2 = 0,1 . 22,4 = 2,24 l
2.24 l < V CO2<3.36 l
C2:
=> n CO2 (1 ) = 0.05 mol , n CO2 (2 ) = 0.075 mol
=> V CO2 = 22,4 . ( 0,05 + 0,075 ) = 2.8 l