Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.
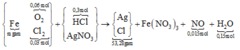
Ghép cụm có nH2O = nO trong oxit + 2nNO
→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa
→ về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
→ Yêu cầu m = mFe = 0,12 × 56 = 6,72 gam.
Đáp án A

Đáp án A
Ta có nHCl cần dùng = 2∑nO trong oxit = 0,24 mol → ∑nHCl đã dùng (dư 25%) = 0,3 mol.
* Gộp cả quá trình có sơ đồ:
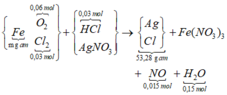
Ghép cụm NO3 bảo toàn O hoặc bảo toàn electron mở rộng ta có:
![]()
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về mặt nguyên tố ∑nAg trong tủa = 0,375 mol.
→ Bảo toàn nguyên tố N có
![]()
Theo đó, m gam Fe ban đầu tương ứng với 0,12 mol → m = 0,12 × 56 = 6,72 gam.

Đáp án A
nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.
Sơ đồ phản ứng
{ Fe (m gam) + (O2 0,06 mol; Cl2 0,03 mol)} + (HCl: 0,3 mol; AgNO3)
→ (Ag-Cl : 53,28 gam) + Fe(NO3)3 + NO 0,015 mol) + H2O 0,15 mol)
Ta có nH2O = nO trong oxit + 2nNO ||→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
||→ m = mFe = 0,12 × 56 = 6,72 gam.
A:Vì
nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.Sơ đồ phản ứng
{ Fe (m gam) + (O2 0,06 mol; Cl2 0,03 mol)} + (HCl: 0,3 mol; AgNO3)
→ (Ag-Cl : 53,28 gam) + Fe(NO3)3 + NO 0,015 mol) + H2O 0,15 mol)
Ta có nH2O = nO trong oxit + 2nNO ||→ nNO = 0,015 mol.∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về nguyên tố nAg trong tủa = 0,375 molBảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.||→ m = mFe = 0,12 × 56 = 6,72 gam.







Đáp án D
2Fe + 3Cl2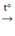 2FeCl3
2FeCl3
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
Chú ý: phản ứng FeCl2 với Cl2 xảy ra khi FeCl2 ở trạng thái dung dịch