Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trong cùng một nhóm A, theo chiều từ trên xuống dưới, bán kính nguyên tử tăng.
Giải thích : Theo chiều từ trên xuống dưới, điện tích hạt nhân tăng nhưng đồng thời số lớp electron cũng tăng và chiếm ưu thế nên kết quả là bán kính nguyên tử tăng theo.

Trong cùng một nhóm A, khi đi từ trên xuống dưới, độ âm điện của các nguyên tử giảm dần.
Giải thích : Trong cùng một nhóm A, khi đi từ trên xuống dưới ; bán kính nguyên tử tăng nên lực hút electron của nguyên tử giảm.

Trong cùng một chu kì, khi đi từ trái sang phải (không xét các khí hiếm), độ âm điện của các nguyên tử tăng.
Giải thích : Trong một chu kì, khi đi từ trái sang phải, điện tích hạt nhàn tăng, bán kính nguyên tử giảm nên lực hút electron của nguyên tử tăng.

Trong cùng một chu kì, tính phi kim của các nguyên tố tăng dần từ trái sang phải.
Trong cùng một nhóm (nhóm A) tính phi kim của các nguyên tố giảm dần từ trên xuống dưới.
Tính kim loại biến thiên ngược chiều với tính phi kim.

- Các electron hóa trị của các nguyên tố thuộc nhóm IA, IIA là electron s. Các nguyên tố đó được gọi là nguyên tố s.
- Các electron hóa trị của các nguyên tố thuộc nhóm IIIA, IVA, VA, VIA, VIIA, VIIIA là các electron s và p. Các nguyên tố đó được gọi là nguyên tố p.
- Số electron thuộc lớp ngoài cùng trong nguyên tử của các nguyên tố s là 1 và 2. Số electron thuộc lớp ngoài cùng trong nguyên tử của các nguyên tố p là 3, 4, 5, 6, 7, 8.

Các nguyên tố thuộc nhóm VIIA gồm các nguyên tố : flo (F), clo (Cl), brom (Br), iot (I), atatin (At). Nguyên tử của chúng có 7 electron hoá trị.
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử góp 1 electron, tạo thành một cặp electron chung tức là một liên kết, vì mỗi nguyên tử chỉ thiếu electron để đạt được cấu hình 8 electron vững bền (giống như của khí hiếm đứng sau nó).
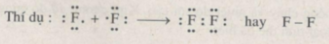

Nhóm A:
- Số thứ tự của nhóm trùng với số electron ở lớp ngoài cùng (cũng đồng thời là số electron hóa trị) của nguyên tử thuộc các nguyên tố trong nhóm.
- Nhóm A có cả nguyên tố thuộc chu kì nhỏ và chu kì lớn.
- Các nguyên tố ở nhóm IA, IIA được gọi là nguyên tố s. Các nguyên tố ở nhóm IIIA đến VIIIA được gọi là nguyên tố p. Trong bảng tuần hoàn, nhóm IA, IIA, IIIA gồm hầu hết các nguyên tố là kim loại, nhóm VA, VIA, VIIA gồm hấu hết các nguyên tố là phi kim. Nhóm VIIIA gồm các khí hiếm.
- Số electron lớp ngoài cùng của nguyên tử thuộc nguyên tố nằm trong từng nhóm A trùng với số thứ tự của nhóm.

- Nhóm IA gồm: H, Li, Na, K, Rb, Cs, Fr.
- Cấu hình electron của các nguyên tố nhóm IA:
H: 1s1 ; Li: 2s1 ; Na: 3 s1 ; K: 4 s1 ; Rb: 5 s1 ; Cs: 6 s1 ; Fr: 7 s1
- Các nguyên tố nhóm IA là các nguyên tố nhóm s, chỉ có 1 electron ở lớp ngoài cùng (ns1).

Khi electron cuối cùng của nguyên tố đó thuộc phân lớp f
khi có e đầu hoặc e cuối trong nhóm f