Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n Fe = a(mol) ; n Mg = b(mol)
=> 56a + 24b = 8(1)
$Mg + 2HCl \to MgCl_2 + H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
n HCl = 2a + 2b = 14,6/36,5 =0,4(2)
Từ (1)(2) => a = b = 0,1
Vậy :
m Fe = 0,1.56 = 5,6(gam)
m Mg = 0,1.24 = 2,4(gam)
n H2 = a + b = 0,2(mol)
V = 0,2.22,4 = 4,48 lít
\(n_{Fe}=a\left(mol\right),n_{Mg}=b\left(mol\right)\)
\(n_{HCl}=\dfrac{14.6}{36.5}=0.4\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
mhh= 56a + 24b = 8 (g)
nHCl = 2a + 2b = 0.4 (mol)
=>a = 0.1
b = 0.1
mFe= 0.1 * 56 = 5.6 (g)
mMg = 2.4 (g)
nH2 = nHCl/2 = 0.4/2 = 0.2 (mol)
VH2 = 0.2*22.4 = 4.48 (l)

\(a)n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ n_{Mg}=\dfrac{4,8}{24}=0,2mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(V_{H_2}=\left(0,1+0,2\right).22,4=6,72l\\ b)V_{ddHCl}=\dfrac{0,2+0,4}{2}=0,3l\\ c)m_{muối}=0,1.127+95.0,2=31,7g\)

a,\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,1 0,2 0,1
b,\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{5,6.100\%}{12}=46,67\%;\%m_{Cu}=100-46,67=53,33\%\)
c,\(m_{HCl}=0,2.36,5=7,3\left(g\right)\Rightarrow m_{ddHCl}=\dfrac{7,3.100}{14,6}=50\left(g\right)\)

Gọi số mol của Zn, Mg và Fe lần lượt là x, y và z mol
TN1: tác dụng với dung dịch HCl tạo 0,5 mol khí H2
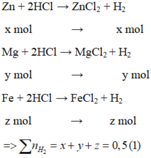
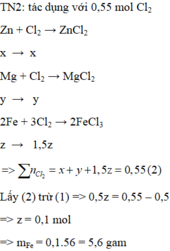
Đáp án: B

Bài 1:
Ta có: \(n_{H_2}=\dfrac{0,4}{2}=0,2\left(mol\right)\)
Bảo toàn Hidro: \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\) \(\Rightarrow m_{HCl\left(p.ứ\right)}=0,4\cdot36,5=14,6\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl\left(p.ứ\right)}-m_{H_2}=24,7\left(g\right)\)

a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ 2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Cho hỗn hợp tác dụng với NaOH, chất rắn không tan là Fe
=> mFe= 1,12 (g) \(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
Ta có: \(n_{H_2\left(2\right)}=n_{Fe}=0,02\left(mol\right)\)
=> \(n_{H_2\left(1\right)}=\Sigma n_{H_2}-n_{H_2\left(2\right)}=0,065-0,02=0,045\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2\left(1\right)}=0,03\left(mol\right)\)
\(\Rightarrow m_{Al}=0,03.27=0,81\left(g\right)\)
\(\Rightarrow\%m_{Al}=41,97\%,\%m_{Fe}=58,03\%\)
b) \(m_{FeCl_2}=0,02.127=2,54\left(g\right)\\ m_{AlCl_3}=0,03.133,5=4,005\left(g\right)\)

Đặt x,y, z lần lượt là số mol của Na,Al,Mg trong m gam hỗn hợp A
m gam A + H2O dư
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
x--------------------x--------->0,5x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x<------x-------------------------------------->1,5x
=> \(0,5x+1,5x=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (1)
2m gam A + NaOH
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
2x------------------------------->x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2y---------------------------------------------->3y
=> \(x+3y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
3m gam A + HCl
\(Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\)
3x--------------------------->1,5x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
3y----------------------------->4,5y
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
3z----------------------------->3z
=> \(1,5x+4,5y+3z=\dfrac{22,4}{22,4}=1\left(mol\right)\) (3)
Từ (1), (2), (3) =>\(\left\{{}\begin{matrix}x=0,05\\y=\dfrac{7}{60}\\z=\dfrac{2}{15}\end{matrix}\right.\)
=> \(m_{Na}=0,05.23=1,15\left(g\right)\)
\(m_{Al}=\dfrac{7}{60}.27=3,15\left(g\right)\)
\(m_{Mg}=\dfrac{2}{15}.24=3,2\left(g\right)\)
=> \(m=1,15+3,15+3,2=7,5\left(g\right)\)
=> \(\%m_{Na}=\dfrac{1,15}{7,5}.100=15,33\%\)
\(\%m_{Al}=\dfrac{3,15}{7,5}.100=42\%\)
\(\%m_{Mg}=\dfrac{3,2}{7,5}.100=42,67\%\)
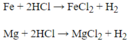
bạn xem lại đề