Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{13}{65}=0,2(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{HCl}=2n_{Zn}=0,4(mol)\\ \Rightarrow m_{HCl}=0,4.36,5=14,6(g)\\ c,n_{H_2}=n_{Zn}=0,2(mol)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48(l)\)
b) mHCl = 14,6 (g)
V H2 = 4,48 (l)
Giải thích các bước:
a) PTHH: Zn + 2HCl → ZnCl2 + H2↑
b) nZn = 13 : 65 = 0,2 mol
Theo PTHH: nHCl = 2.nZn = 0,4 mol
mHCl = 0,4 . 36,5 = 14,6(g)
c) nH2 = nZn = 0,2 mol
VH2 = 0,2 . 22,4 = 4,48 (l)

\(n_{HCl}=0,25.2=0,5\left(mol\right)\\ a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ b,n_{Zn}=n_{H_2}=n_{ZnCl_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\\ m_{Zn}=0,25.65=16,25\left(g\right)\\ c,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)
Không biết đúng không nữa;-;;;
a) PTHH: Zn + 2HCl -> ZnCl2 + H2
b) HCl=250ml=0,25l
n2HCl= V/22,4= 0,5/22,4= 0,02(mol)
Zn + 2HCl -> ZnCl2 + H2
1 2 1 1
0,01 <-0,5--------------> 0,01
mZn= n.M= 0,01.65= 0,65(gam)
c) VH2=n . 22,4= 0,01 . 22,4= 0,224(l)

a.b.c.\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2 ( mol )
\(m_{ZnCl_2}=n.M=0,2.136=27,2g\)
\(V_{H_2}=n.22,4=0,2.22,4=4,48l\)
d.\(n_{CuO}=\dfrac{m}{M}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,4 > 0,2 ( mol )
0,2 0,2 0,2 ( mol )
\(m_{chất.rắn}=m_{CuO\left(dư\right)}+m_{Cu}=0,2.80+0,2.64=16+12,8=28,8g\)
\(\%m_{CuO}=\dfrac{16}{28,8}.100=55,55\%\)
\(\%m_{Cu}=100\%-55,55\%=44,45\%\)

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,\text {Bảo toàn KL: }m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Rightarrow m_{ZnCl_2}=6,5+7,3-0,2=13,6(g)\)

a) Zn + 2HCl →ZnCl2 + H2
b) nZn = 6,5/65 = 0,1 mol . Theo tỉ lệ pư => nH2 = nZn = nZnCl2 =0,1 mol <=> VH2(đktc) = 0,1.22,4 = 2,24 lít.
c) mZnCl2 = 0,1 . 136 = 13,6 gam
d) nHCl =2nZn = 0,2 mol => mHCl = 0,2.36,5= 7,3 gam
Cách 2: áp dụng định luật BTKL => mHCl = mZnCl2 + mH2 - mZn
<=> mHCl = 13,6 + 0,1.2 - 6,5 = 7,3 gam

`a)PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`n_[HCl]=0,2.1=0,2(mol)`
`=>m_[Zn]=0,1.65=6,5(g)`
`b)m_[dd HCl]=1,1.200=220(g)`
`=>C%_[ZnCl_2]=[0,1.136]/[6,5+220-0,1.2].100~~6%`
\(a,n_{HCl}=0,2.1=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1<--0,2------>0,1------->0,1
\(\rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
\(b,m_{ddHCl}=200.1,1=220\left(g\right)\)
\(\rightarrow m_{dd}=220+6,5-0,1.2=226,3\left(g\right)\\ \rightarrow C\%_{ZnCl_2}=\dfrac{0,1.136}{226,3}.100\%=6\%\)

\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Áp dung định luật BTKL :
\(m_{H_2}=13+14.6-27.2=0.4\left(g\right)\)
\(n_{H_2}=\dfrac{0.4}{2}=0.2\left(mol\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)

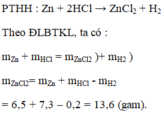
Zn+2HCl-->ZnCl2+H2
0,3---0,6-------0,3-------0,3
=>mZn=0,3.65=19,5 g
=>mHCl=0,6.36,5=21,8g
=>mZnCl2=0,3.136=40,8 g
=áp dụng định luật bảo toang khối lượng
=>mZn+mHCl=mZnCl2+mH2
=>mZnCl=19,5+21,8-(0,3.2)=40,8 g
.