Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 14 :
Trích mẫu thử :
Cho quỳ tím vào từng mẫu thử :
+ Hóa đỏ : HCl , H2SO4
+ Không đổi màu : NaNO3
Cho dung dịch BaCl2 vào 2 mẫu thử làm quỳ tím hóa đỏ :
+ Chất nào xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt

- Trích mẫu thử.
- Cho từng mẫu thử pư với nhau.
| Na2CO3 | Ba(HCO3)2 | NaHSO4 | KHCO3 | Mg(HCO3)2 | |
| Na2CO3 | - | ↓ | ↑ | - | ↓ |
| Ba(HCO3)2 | ↓ | - | ↑↓ | - | - |
| NaHSO4 | ↑ | ↑↓ | - | ↑ | ↑ |
| KHCO3 | - | - | ↑ | - | - |
| Mg(HCO3)2 | ↓ | - | ↑ | - | - |
+ Mẫu thử tạo 2 pư có kết tủa và 1 pư sủi bọt khí: Na2CO3.
+ Mẫu thử tạo 1 pư có kết tủa và 1 pư vừa có kết tủa vừa sủi bọt khí: Ba(HCO3)2
+ Mẫu thử tạo 1 pư vừa có kết tủa vừa sủi bọt khí và 3 pư sủi bọt khí: NaHSO4
+ Mẫu thử tạo 1 pư sủi bọt khí: KHCO3
+ Mẫu thử tạo 1 pư có kết tủa và 1 pư sủi bọt khí: Mg(HCO3)2.
- Dán nhãn.
PT: \(Na_2CO_3+Ba\left(HCO_3\right)_2\rightarrow2NaHCO_3+BaCO_{3\downarrow}\)
\(Na_2CO_3+2NaHSO_4\rightarrow2Na_2SO_4+CO_2+H_2O\)
\(Na_2CO_3+Mg\left(HCO_3\right)_2\rightarrow2NaHCO_3+MgCO_{3\downarrow}\)
\(Ba\left(HCO_3\right)_2+2NaHSO_4\rightarrow BaSO_{4\downarrow}+Na_2SO_4+2CO_2+2H_2O\)
\(2NaHSO_4+2KHCO_3\rightarrow Na_2SO_4+K_2SO_4+2CO_2+2H_2O\)
\(2NaHSO_4+Mg\left(HCO_3\right)_2\rightarrow Na_2SO_4+MgSO_4+2CO_2+2H_2O\)

Trích mẫu thử, cho quỳ tím vào các mẫu thử:
- Quỳ hóa xanh: \(NaOH,Ba(OH)_2\)
- Quỳ ko đổi màu: \(NaNO_3\)
Sục khí \(CO_2\) vào mẫu thử làm quỳ hóa xanh, sau p/ứ tạo KT trắng là \(Ba(OH)_2\), ko ht là \(NaOH\)
\(Ba(OH)_2+CO_2\to BaCO_3\downarrow+H_2O\)

- Viết phương trình hoá học của phản ứng giữa Mg với các dung dịch CuSO 4 , FeSO 4 và AgNO 3 .
Mg + FeSO 4 → MgSO 4 + Fe
Mg + CuSO 4 → MgSO 4 + Cu
Mg + AgNO 3 → Mg NO 3 2 + Ag
- Viết phương trình hoá học của phản ứng giữa Fe với các dung dịch CuSO 4 , AgNO 3
Fe + CuSO 4 → FeSO 4 + Cu
Fe + 2 AgNO 3 → Fe NO 3 2 + 2Ag
- Viết phương trình hoá học của phản ứng giữa Cu với dung dịch AgNO 3
Cu + AgNO 3 → Cu NO 3 2 + Ag

- Trích một ít các dd làm mẫu thử, đánh số thứ tự lần lượt
- Cho các dd tác dụng với giấy quỳ tím:
+ QT chuyển đỏ: HCl
+ QT chuyển xanh: NaOH
+ QT không chuyển màu: KCl, NaNO3 (I)
- Cho dd ở (I) tác dụng với dd AgNO3:
+ Không hiện tượng: NaNO3
+ Kết tủa trắng: KCl
\(KCl+AgNO_3\rightarrow AgCl\downarrow+KNO_3\)

- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ hóa đỏ: HCl
+ Quỳ không đổi màu: NaCl, Na2SO4 (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: Na2SO4
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)
+ Không hiện tượng: NaCl
- Dán nhãn.

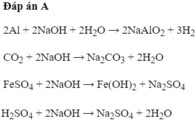
_ Có 8 cặp chất xảy ra pư.
PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Mg+CuSO_4\rightarrow MgSO_4+Cu\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(H_2SO_4+BaCl_2\rightarrow BaSO_{4\downarrow}+2HCl\)
\(CuSO_4+2NaOH\rightarrow Na_2SO_4+Cu\left(OH\right)_{2\downarrow}\)
\(CuSO_4+BaCl_2\rightarrow CuCl_2+BaSO_{4\downarrow}\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
Bạn tham khảo nhé!