Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 1:
các chất có thể tác dụng với nhau từng đôi một
KOH với HCl: KOH + HCl ➝ KCl + H2O
KOH với H2SO4 loãng: 2KOH + H2SO4 ➝ K2SO4 + 2H2O
KOH với AL2O3: 2KOH + Al2O3 ➝ 2KAlO2 + H2O
KOH với khí CO2: 2KOH + CO2 ➝ K2CO3 + H2O
hoặc KOH + CO2 ➝ KHCO3
HCl với Fe(OH)3: 6HCl + 2Fe(OH)3 ➝ 2FeCl3 + 6H2O
HCl với Al2O3: 6HCl + Al2O3 ➝ 2AlCl3 + 3H2O
H2SO4 với Fe(OH)3: 3H2SO4 + 2Fe(OH)3 ➝ Fe2(SO4)3 + 6H2O
câu 2:
HCl và H2SO4 loãng tác dụng được với kim loại tạo muối và khí H2:
HCl + Zn ➝ ZnCl2 + H2↑
H2SO4 + Zn ➝ ZnSO4 + H2↑
HCl và H2SO4 loãng tác dụng với oxit kim loại tạo muối và nước:
HCl + MgO ➝ MgCl2 + H2O
MgO + H2SO4 ➝ MgSO4 + H2O
còn lại là tương tự bạn tự giải nha ^^

Trích mỗi dd một ít, đánh STT làm mẫu thử.
*Cho mẩu quỳ tím vào từng dd
- Hóa đỏ: HCl, H2SO4
- Hóa xanh: NaOH, Ba(OH)2
- Không đổi màu: K2SO4
* Cho K2SO4 vào 2 mẫu thử làm quỳ tím hóa xanh.
- Mẫu thử xuất hiện kết tủa trắng: Ba(OH)2
Ba(OH)2 + K2SO4 --> 2KOH + BaSO4↓
- Mẫu thử KHT: NaOH
* Cho Ba(OH)2 vào 2 mẫu thử làm quỳ tím hóa đỏ
- Mẫu thử xuất hiện kết tủa trắng là H2SO4
Ba(OH)2 + H2SO4 --> 2H2O + BaSO4↓
- Mẫu thử KHT là HCl
Ba(OH)2 + 2HCl --> 2H2O + BaCl2

a) không phản ứng
b)
* Nếu KOH dư tạo muối trung hoà
2KOH + CO2 → K2CO3 + H2O
* Nếu CO2 dư tạo muối axit
KOH + CO2 → KHCO3
c) không phản ứng
d)
* Nếu Ba(OH)2 dư tạo muối trung hoà
Ba(OH)2 + CO2 → BaCO3+ H2O
* Nếu CO2 dư tạo muối axit
Ba(OH)2 +2CO2 → Ba(HCO3)2

1. \(n_{NaOH}=\dfrac{32}{40}=0,8\left(mol\right);n_{H_2SO_4}=\dfrac{245.20\%}{98}=0,5\left(mol\right)\)
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+H_2O\)
Đề: 0,5.......0,8
Lập tỉ lệ : \(\dfrac{0,5}{1}>\dfrac{0,8}{2}\)=> H2SO4 dư, NaOH hết
\(m_{Na_2SO_4}=\dfrac{0,8}{2}.142=56,8\left(g\right)\)
\(C\%_{Na_2SO_4}=\dfrac{56,8}{32+245}.100=20,51\%\)
\(C\%_{H_2SO_4}=\dfrac{\left(0,5-0,4\right).98}{32+245}.100=3,54\%\)

-Dùng quỳ tím nhận biết được ba nhóm:
Nhóm axit:H2SO4,HCl do làm quỳ đổi màu đỏ
Nhóm bazơ do làm quỳ đổi màu xanh:Ba(OH)2,NaOH
-Nhóm axit,dùng BaO tác dụng với 2 dd axit,nhận ra H2SO4 do BaSO4 kết tủa trắng.Phản ứng còn lại không có chất kết tủa
PTHH:BaO+H2SO4->BaSO4(kết tủa)+H2O
BaO+2HCl->BaCl2+H2O
-Nhóm ba zơ:dùng dd H2SO4(loãng) ở trên cho tác dụng với hỗn hợp 2 dd ba zơ,nhận ra Ba(OH)2 do BaSO4 kết tủa trắng,còn Na2SO4 tan trong dd
PTHH:2NaOH+H2SO4->Na2SO4+2H2O
Ba(OH)2+H2SO4->BaSO4(kết tủa)+2H2O
- Lấy mẫu thử và đánh dấu
- Cho quỳ tím và các mẫu thử
+ Mẫu thử làm quỳ tím hoá đỏ chất ban đầu là HCl, H2SO4 (I)
+ Mẫu thử làm quỳ tím hoá xanh chất ban đầu là NaOH, Ba(OH)2 (II)
- Cho chất nhóm I vào nhóm II
+ Mẫu thử xuất hiện kết tủa trắng chất ban đầu là Ba(OH)2 và H2SO4
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
+ Mẫu thử không có hiện tượng chất ban đầu là HCl và NaOH
HCl + NaOH → NaCl + H2O

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

a. Pt: CuO+2HNO3--> Cu(NO3)2 + H2O
b. Ta có nCuO=\(\dfrac{12}{80}=0,15mol\)
Theo pt nCuO:nHNO3=1:2
=>nHNO3=0,3 mol
=>mHNO3 p/ứ=0,3.(1+14+16.3)=18,9g
c.mdd=12+200=212g
mchất tan HNO3=\(\dfrac{15,5.200}{100}=31g\)
mHNO3 dư= 31-18,9=12,1g
Theo phương trình nCuO=nCu(NO3)2
=>nCu(NO3)2= 0,15 mol
=>mCu(NO3)2=0,15.188=28,2g
%Cu(NO3)2=\(\dfrac{28,2}{212}.100=13,3\%\)
%HNO3 dư=\(\dfrac{12,1}{212}.100=5,7\%\)
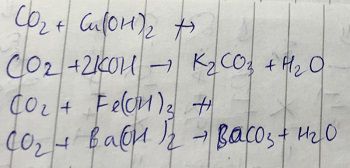
Na2CO3 + 2HCl →2NaCl + CO2+ H2O
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Na2CO3 + Ba(NO3)2 → 2NaNO3 + BaCO3
Na2CO3 + Mg(OH)2 → 2NaOH + MgCO3
CaCO3 +2HCl → CaCl2 + CO2 +H2O
K2SO4 + Ba(OH)2 → 2KOH + BaSO4
K2SO4 + Ba(NO3)2 → 2KNO3 + BaSO4
2HCl + Ba(OH)2 → BaCl2 + 2H2O
2HCl + Ba(NO3)2 →BaCl2 + 2HNO3
2HCl + Mg(OH)2 → MgCl2 + 2H2O