
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

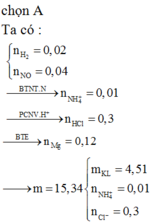

Đáp án B
Theo giả thiết, suy ra trong Y có NO (khí không màu hóa nâu trong không khí).
Mặt khác, ![]() khí còn lại trong Y là H2. Vì đã có H2 sinh ra nên
NO
3
-
không còn trong dung dịch X.
khí còn lại trong Y là H2. Vì đã có H2 sinh ra nên
NO
3
-
không còn trong dung dịch X.
Theo giả thiết, bảo toàn nguyên tố N, bảo toàn electron, ta có :


Đáp án B
Hai khí thu được không màu, có một khí hóa nâu trong không khí là NO.
M Y = 2 . 12 , 2 = 24 , 4 < M NO => Chứng tỏ khí còn lại trong Y có PTK nhỏ hơn 24,4 => Đó là H2.
Đặt a, b lần lượt là số mol NO và H2

Vì phản ứng có tạo khí H2 nên NO 3 - đã phản ứng hết mà n NO < n NO 3 - => có muối amoni tạo thành, n NH 4 + = 0 , 05 + 0 , 1 - 0 , 1 = 0 , 05 mol
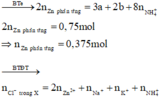
⇒ n Cl - trong X = 2 . 0 , 375 + 0 , 05 + 0 , 1 + 0 , 05 = 0 , 95 mol ⇒ m = m cation + m animon = 65 . 0 , 375 + 23 . 0 , 05 + 39 . 0 , 1 + 18 . 0 , 05 + 35 , 5 . 0 , 95 = 64 , 05 g

Đáp án B
NO3- phản ứng hết
Giả sử nNH4+ = x mol
+ BTNT N: nNH4++nNO = nNaNO3+nKNO3 => x+0,1 = 0,05+0,1 => x=0,05 mol
+ BT electron => nZn = (3nNO+2nH2+8nNH4+)/2=(3.0,1+2.0,025+8.0,05)/2=0,375 mol
+ BTĐT: nCl-=(2nZn2+ + nNa+ + nK+ + nNH4+) = (2.0,375+0,05+0,1+0,05)=0,95 mol
Dung dịch X gồm:
0,375 mol Zn2+
0,05 mol Na+
0,1 mol K+
0,05 mol NH4+
0,95 mol Cl-
=>m=0,375.65+0,05.23+0,1.39+0,05.18+0,95.35,5=64,05 g

Khí không màu hóa nâu trong kk là NO. Vì tỷ khối của 2 khí là 24,4 nên có 1 khí là H2
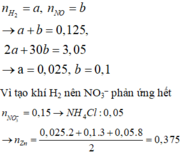
⇒ mMuối = mZnCl2 + mNH4Cl + mNaCl + mKCl = 64,05 gam
Đáp án C

Đáp án C
Khí không màu hóa nâu trong kk là NO.
Vì tỷ khối của 2 khí là 24,4 nên có 1 khí là H2
![]()
![]()
Vì tạo khí H2 nên NO3– phản ứng hết
![]()
![]()
⇒ mMuối = mZnCl2 + mNH4Cl + mNaCl + mKCl = 64,05 gam

Giải thích:
Vì Mx = 12,2.2 = 24,4 hỗn hợp khí là NO và H2

Al + 4H+ + NO3- → Al3+ + NO + H2O
0,1 ← 0,4 ← 0,1 ← 0,1
2Al + 6H+ → 2Al3+ + 3H2
1/60 ← 0,05 ← 0,025
Bảo toàn khối lượng m = m Al + m Na+ + m K+ + m NO3- + m Cl-
= ( 0,1 + 1/60) .27 + 23. 0,05 + 0,1.39 + (0,15 – 0,1). 62 + 0,45.35,5
= 27,275 (g)
Đáp án B