K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

11 tháng 4 2017
Giả thiết cả 2 lần dùng NaOH thì kết tủa đều tan 1 phần
=> Do n↓ (1)= 2 n↓ (2)
=> 4nAl3+ - nOH- (1) = 2(4nAl3+ - nOH- (2) )
=> nAl3+ = ¼ (2.nOH- (2) - nOH- (1) ) = 0,11 mol
=> m = m Al2(SO4)3 = 18,81g
=>C

30 tháng 3 2017
Đáp án C
nNaOH (1) = 0,48 mol
nNaOH (2) = 0,51 mol
Gọi số mol A13+ trong m gam A1C13 là X
Coi 4a, 3a là số mol của Al(OH)3


18 tháng 2 2017
Đáp án : D
, nHCl = 0,3 mol ; nNaOH = 0,32 mol ; nAl(OH)3 = 0,06 mol
Vì nNaOH > nHCl => dư OH sau khi phản ứng hết với AlCl3 => có hiện tượng hòa tan kết tủa
=> nOH tan kết tủa = nNaOH – nHCl = 0,02 mol
=> nAl(OH)3 max = 0,06 + 0,02 = 0,08 mol = nAl bđ
=> mAl = 2,16g
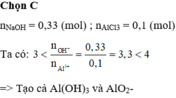
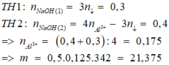







Đáp án C
n H C l = 0 , 2 m o l
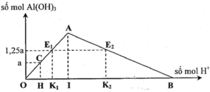
Nếu cho 0,65 mol NaOH vào X thì thu được 2m gam kết tủa còn nếu thêm 0,925 mol NaOH thì thu được m gam kết tủa. Chứng tỏ lúc cho 0,925 mol NaOH thì có sự hòa tan kết tủa.
Khi cho 0,65 mol NaOH tác dụng với X thì chỉ có 0,45 mol NaOH tác dụng với AlCl3 còn khi cho 0,925 mol thì có 0,725 mol tác dụng.
Nhận thấy 0,925-0,45>0,45 do vậy lúc cho 0,65 mol NaOH thì chưa hòa tan kết tủa.
n A l ( O H ) 3 = 0 , 45 3 = 0 , 15 m o l
Do vậy lúc cho 0,925 mol NaOH thì thu được 0,075 mol kết tủa.
→ n A l C l 3 = 0 , 725 - 0 , 075 . 3 4 + 0 , 075 = 0 , 2 m o l → a = 26 , 7 g a m