Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có nMg=0,145 mol
Gọi x và y lần lượt là số mol của H2 và N2
Ta có: x+ y= 0,025; 2x+ 28y= 0,025.(11,4.2) → x= 0,005; y= 0,02
Vì có khí H2 thoát ra → NO3- hết → Muối thu được là muối clorua
QT cho e:
Mg → Mg2++ 2e (1)
0,145→ 0,29 mol
QT nhận e:
2N+5+ 10e →N2 (2)
0,2← 0,02 mol
2H+1+2e→ H2 (3)
0,01← 0,005 mol
Nếu chỉ có quá trình nhận (2) và (3) thì
ne nhận= 0,2+ 0,01= 0,21 mol≠ 0,29 mol
→ Còn có quá trình nhận e tạo muối NH4+
Theo ĐL bảo toàn e: ne cho=n e nhận= 0,29 mol → e nhận ở (4)= 0,29-0,21=0,08 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,08 → 0, 01 mol
Bảo toàn nguyên tố N ta có
nN(KNO3)= nN(N2)+ nN (NH4+)=2.0,02+ 0,01= 0,05 mol= nKNO3= nK+
Muối chứa Mg2+: 0,145 mol, NH4+: 0,01 mol, K+: 0,05 mol, Cl-
Dùng bảo toàn điện tích: 0,145.2+ 0,01.1+ 0,05= nCl-= 0,35 mol
→mmuối=m= 0,145.24+ 0,01.18+ 0,05.39+ 0,35.35,5= 18,035 gam
Đáp án D

Chọn D

Vì có khí H 2 thoát ra và Zn dư → H + và NO 3 - hết → Muối thu được là muối clorua.
Do n NO 3 - ban đầu = 0,15 mol > n NO = 0,09 mol→ X chứa NH 4 + .
Bảo toàn nguyên tố N → n NH 4 + = 0,15- 0,09= 0,06(mol)
Bảo toàn electron: 2. n Zn pứ = 3. n NO + 8 n NH 4 + + 2 n H 2 → n Zn pứ = n Zn 2 + = 0,405 mol
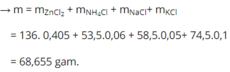




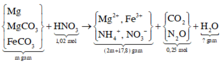
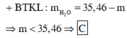

Đáp án C
Từ nHỗn hợp 2 khí và khối lượng 2 khí
⇒ nN2 = 0,01 và nH2 = 0,1 mol.
Bảo toàn e ta có nNH4+ = = 0,025 mol.
= 0,025 mol.
⇒ nHCl = 12nN2 + 2nH2 + 10nNH4+ = 0,69 mol.
+ Bảo toàn điện tích hoặc bảo toàn nitơ
⇒ nK+ = 0,065 mol.
⇒ mMuối = 0,3×24 + 0,065×39 + 0,025×18 + 0,69×35,5
= 34,68 gam.