Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
2107 gam dung dịch H2SO4 loãng, nồng độ 10% gồ 2,15 mol chất tan H2SO4 và 189,3 gam H2O.
→ kết quả cô cạn dung dịch Y thu được 1922,4 gam H2O là gồm lượng sẵn có trên là lượng sinh ra thêm do phản ứng giữa X + H 2 SO 4 ⇒ lượng sinh thêm là 26,1 gam ⇄ 1,45mol
*Sơ đồ phản ứng:
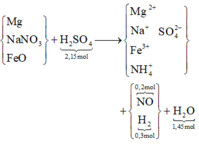
Có sơ đồ, việc giải bài tập trở nên đơn giản, chỉ là thuần “ban bật” bảo toàn nguyên tố qua dấu “ → ”:
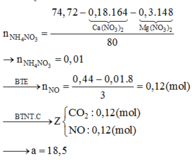
Thật vậy, bảo toàn nguyên tố H có 0,2 mol NH 4 + → có 0,4 mol NaNO3 theo bảo toàn nguyên tố N.
Bỏ góc SO4 hai vế rồi bảo toàn nguyên tố O có 0,45 mol
![]()
Mà oxi chiếm 26,4% khối lượng X nên
![]()
Biết lượng FeO, NaNO3 rồi nên suy ra lượng còn lại 33,6 gam là của Mg.
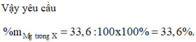

Đáp án B
Sơ đồ quá trình:
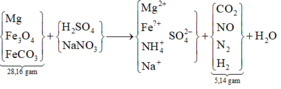

Đặt câu hỏi: 1,285 mol Na trong NaOH thêm vào và Na trong NaNO3 sẵn có cuối cùng đi về đâu?
À, về hết trong 0,715 mol Na2SO4 → số mol NaNO3 ban đầu là 0,715 x 2 – 1,285 = 0,415 mol
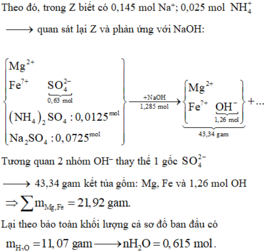
Giải hệ hỗn hợp khí Y gồm CO2, N2, NO và 0,05 mol H2; biết tổng mol Y là 0,2; nặng 5,14 gam.


Chọn đáp án A.
Khí trong Z hóa nâu ngoài không khí là NO.
M Z = 4 , 5 . 4 = 18 < M NO => Khí còn lại có PTK < 18 => Khí đó là H2.

Đặt số mol của Mg, Al, ZnO lần lượt là x, y, z
Có khí H2 thoát ra nên sau phản ứng số mol Fe2+ không đổi.



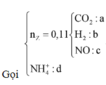
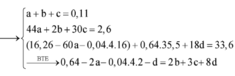
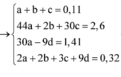
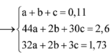
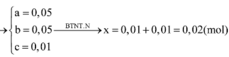

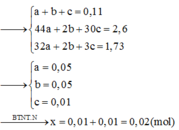
Đáp án B
Dùng phương pháp đường chéo tính được mol CO2 là 0,2 mol và H2 là 0,15 mol.