Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

\(n_{Fe}=\dfrac{m}{M}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
1 : 2 : 1 (mol)
0,05 : 0,4 (mol)
-Chuyển thành tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,4}{2}\Rightarrow\) Fe phản ứng hết còn HCl dư.
-Theo PTHH: \(n_{H_2}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
b) \(n_{Fe\left(cần\right)}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(\Rightarrow n_{Fe\left(thêm\right)}=n_{Fe\left(cần\right)}-n_{Fe\left(tt\right)}=0,2-0,05=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(thêm\right)}=n.M=0,15.56=8,4\left(g\right)\)

a. \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b. \(n_{Mg}=\dfrac{2.4}{24}=0.1mol\)
\(mct_{HCl}=\dfrac{500\times36.5}{100}=182.5g\Rightarrow n_{HCl}=\dfrac{182.5}{36.5}=5mol\)
Ta có: \(\dfrac{0.1}{1}< \dfrac{5}{2}\Rightarrow\) HCl dư
nHCl phản ứng = 0.2 mol => nHCl dư = 5 - 0.2 = 4.8 mol
mHCl dư = \(4.8\times36.5=175.2g\)
c. \(V_{H_2}=0.1\times22.4=2.24l\)
d. mdd sau phản ứng = \(2.4+500-0.1\times2=502.2g\)
\(C\%_{MgCl_2}=\dfrac{0.1\times95\times100}{502.2}=1.89\%\)

1.
a, \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,15 0,3
b, Ta có: \(\dfrac{0,15}{1}< \dfrac{0,5}{2}\) ⇒ Mg pứ hết, HCl dư
\(m_{HCldư}=\left(0,5-0,3\right).36,5=7,3\left(g\right)\)
c, \(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
2.
a, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 ---to→ 2P2O5
Mol: 0,2 0,25 0,1
b, \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c, \(m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(V_{kk}=5,6.5=28\left(l\right)\)

\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 < 0,4 ( mol )
0,1 0,2 0,1 0,1 ( mol )
Chất dư là HCl
\(m_{HCl\left(dư\right)}=\left(0,4-0,2\right).36,5=7,3g\)
\(V_{H_2}=0,1.22,4=2,24l\)
\(m_{FeCl_2}=0,1.127=12,7g\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\
n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\\
pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(LTL:\dfrac{0,1}{1}< \dfrac{0,4}{1}\)
=> H2SO4 d
\(n_{H_2SO_4\left(pu\right)}=n_{Fe}=0,1\left(mol\right)\\
m_{H_2SO_4\left(d\right)}=\left(0,4-0,1\right).98=29,4g\)
\(n_{H_2}=n_{FeSO_4}=n_{Fe}=0,1\left(mol\right)\)
\(V_{H_2}=0,1.22,4=2,24l\\
m_{FeSO_4}=0,1.152=15,2g\)

a, \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 -----> FeSO4 + H2
b, ko tính đc do thiếu khối lượng ddH2SO4
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
nFe = 5,6 : 56 = 0,1 (mol)
nH2SO4 (đủ) = 0,1 (mol)
mH2SO4 = 0,1 . 98 = 9,8 (g)
\(mH_2SO_{\text{4(thamgiapứ) }}=\dfrac{9,8.100}{49}=20\left(g\right)\)
H2SO4 dư , Fe đủ
mH2SO4 dư = 20 - 9,8 = 10,2(g)
mFeSO4 = 0,1 . 152 = 15,2(g)
VH2 = 0,1 .22,4 = 2,24(l)
mH2 = 0,1 . 2 = 0,2 (g)
\(C\%H_2SO_4=\dfrac{10,2.100}{5,6+20+15,2-0,2}=25\%\)
\(C\%_{FeSO_4}=\dfrac{15,2.100}{5,6+20+15,2-0,2}=37\%\)
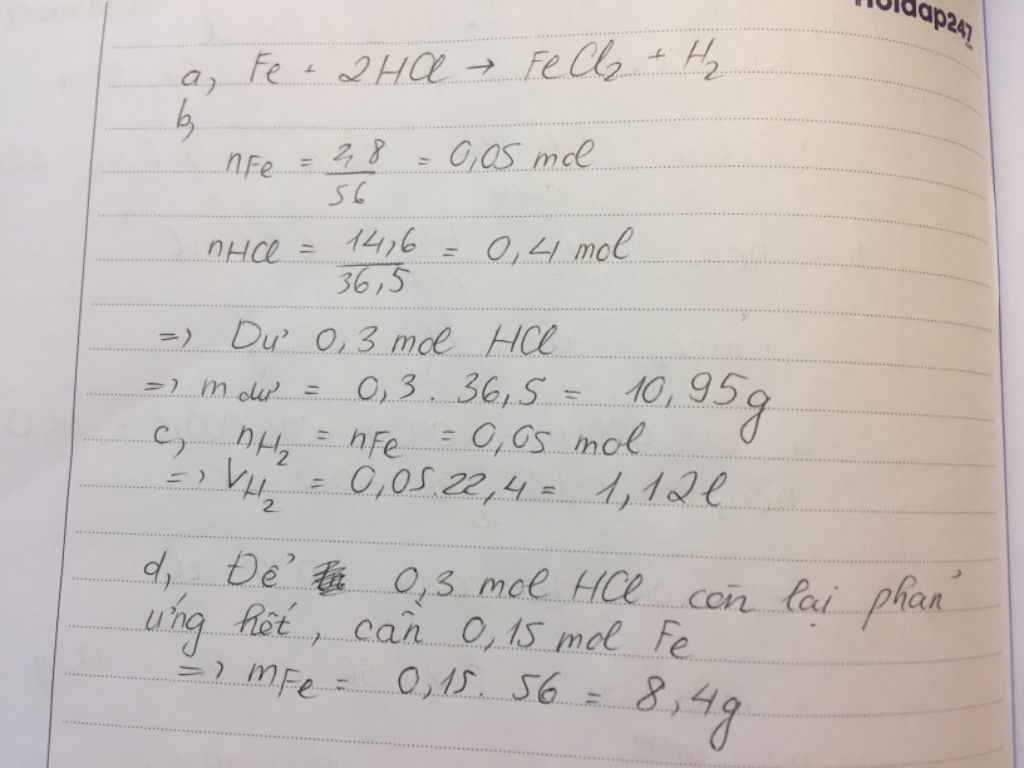

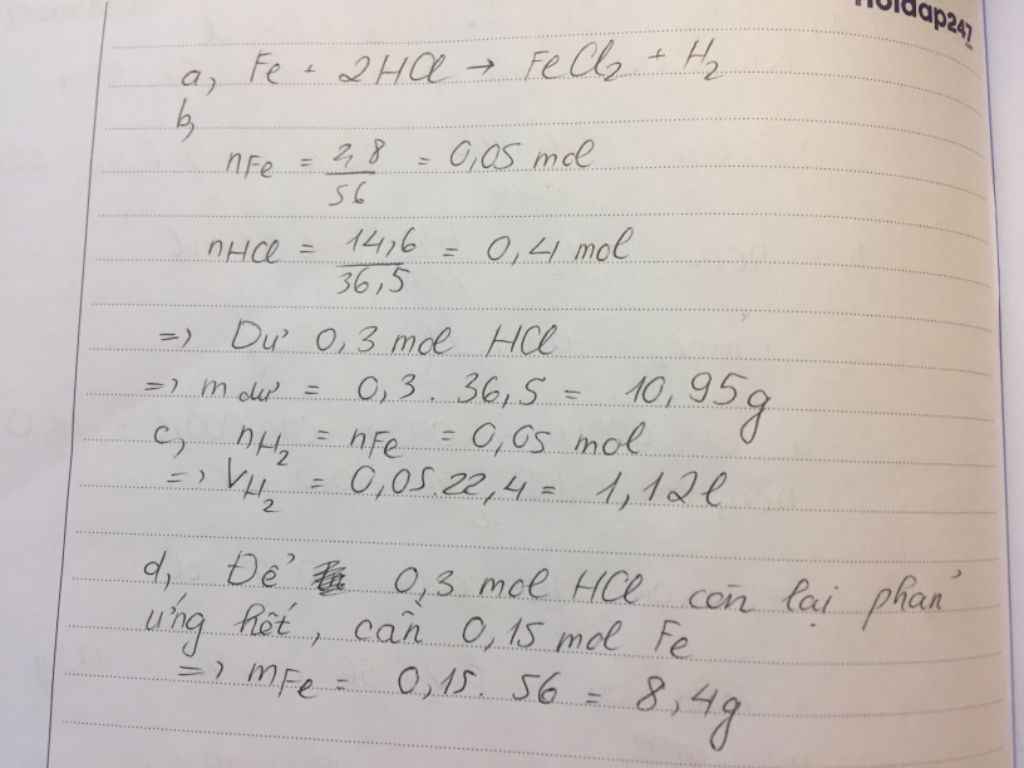
\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\\ n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
LTL: \(0,05< \dfrac{0,4}{2}\rightarrow\) HCl dư
Theo pthh: \(\left\{{}\begin{matrix}n_{H_2}=n_{Fe}=0,05\left(mol\right)\\n_{HCl\left(pư\right)}=2n_{Fe}=0,05.2=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}V_{H_2}=0,05.22,4=1,12\left(l\right)\\m_{HCl\left(dư\right)}=\left(0,4-0,1\right).36,5=10,95\left(g\right)\end{matrix}\right.\)
Theo pthh: \(n_{Fe\left(thêm\right)}=\dfrac{1}{2}n_{HCl\left(dư\right)}=\dfrac{1}{2}.\left(0,4-0,1\right)=0,15\left(mol\right)\)
\(\rightarrow m_{Fe\left(thêm\right)}=0,16.56=8,4\left(g\right)\)