Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

Fe+2Hcl->FeCl2+H2
0,1---------------------0,1
2H2+O2-to>2H2O
0,1--------------0,1
n Fe=0,1 mol
=>VH2=0,1.22,4=2,24l
c) m H2O=0,1.18.95%=1,71g
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
0,1 0,1
2H2 + O2 --to--> 2H2O
0,1 0,1
\(\rightarrow\left\{{}\begin{matrix}V_{H_2}=0,1.22,4=2,24\left(l\right)\\m_{H_2O}=0,1.18.\left(100\%-5\%\right)=1,71\left(g\right)\end{matrix}\right.\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl ---> MgCl2 + H2
0,2 0,2
2H2 + O2 --to--> 2H2O
0,2 0,2
\(\rightarrow\left\{{}\begin{matrix}V_{H_2}=0,2.22,4=4,48\left(l\right)\\m_{H_2O}=0,2.18.\left(100\%-5\%\right)=3,42\left(g\right)\end{matrix}\right.\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,2
\(V_{H_2}=0,2\cdot22,4=4,48l\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,2 0,2
\(m_{H_2O}=0,2\cdot18\cdot\left(100-5\right)\%=3,42g\)

a) Zn + 2HCl --> ZnCl2 + H2
b) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2------------------->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
c) \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,2}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,2<--0,2
=> mCuO(Dư) = (0,3 - 0,2).80 = 8 (g)

a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
____0,2____________0,2____0,2 (mol)
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
c, \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\), ta được H2 dư.
Theo PT: \(n_{Cu}=n_{CuO}=0,1\left(mol\right)\Rightarrow m_{cr}=m_{Cu}=0,1.64=6,4\left(g\right)\)

a, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, Có lẽ đề hỏi bao nhiêu gam đồng thay vì "bao nhiêu gam sắt" bạn nhỉ?
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)

a)
n Al = 10,8/27 = 0,4(mol)
2Al + 6HCl → 2AlCl3 + 3H2
n H2 = \(\dfrac{3}{2}\)n Al = 0,6(mol)
=> V H2 = 0,6.22,4 = 13,44(lít)
b) n AlCl3 = n Al = 0,4(mol)
=> m AlCl3 = 0,4.133,5 = 53,4(gam)
c) n CuO = 16/80 = 0,2(mol)
CuO + H2 \(\xrightarrow{t^o}\) Cu + H2O
n CuO = 0,2 < n H2 = 0,6 => H2 dư
n H2 pư = n Cu = n CuO = 0,2 mol
Suy ra:
m H2 dư = (0,6 -0,2).2 = 0,8(gam)
m Cu = 0,2.64 = 12,8(gam)
a) nAl=0,4(mol)
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
nH2= 3/2 . nAl=3/2 . 0,4=0,6(mol)
=>V(H2,đktc)=0,6 x 22,4= 13,44(l)
b) nAlCl3= nAl=0,4(mol)
=>mAlCl3=133,5 x 0,4= 53,4(g)
c) nCuO=0,2(mol)
PTHH: CuO + H2 -to-> Cu + H2O
Ta có: 0,2/1 < 0,6/1
=> H2 dư, CuO hết, tính theo nCuO
=> nH2(p.ứ)=nCu=nCuO=0,2(mol)
=>nH2(dư)=0,6 - 0,2=0,4(mol)
=> mH2(dư)=0,4. 2=0,8(g)
mCu=0,2.64=12,4(g)
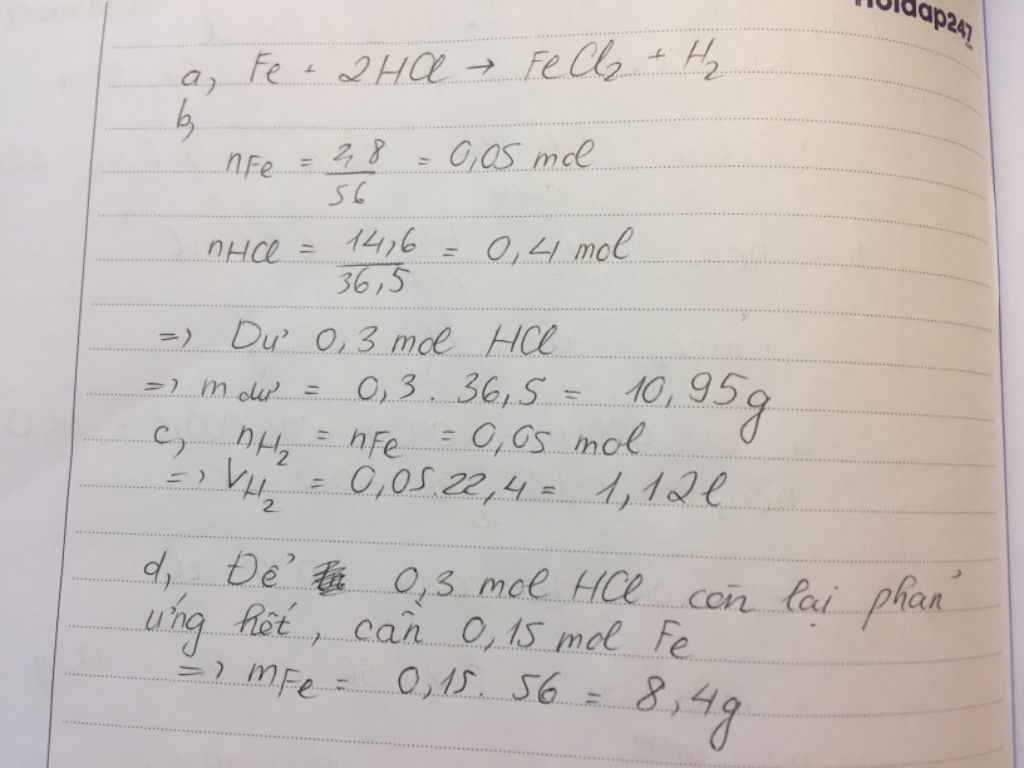
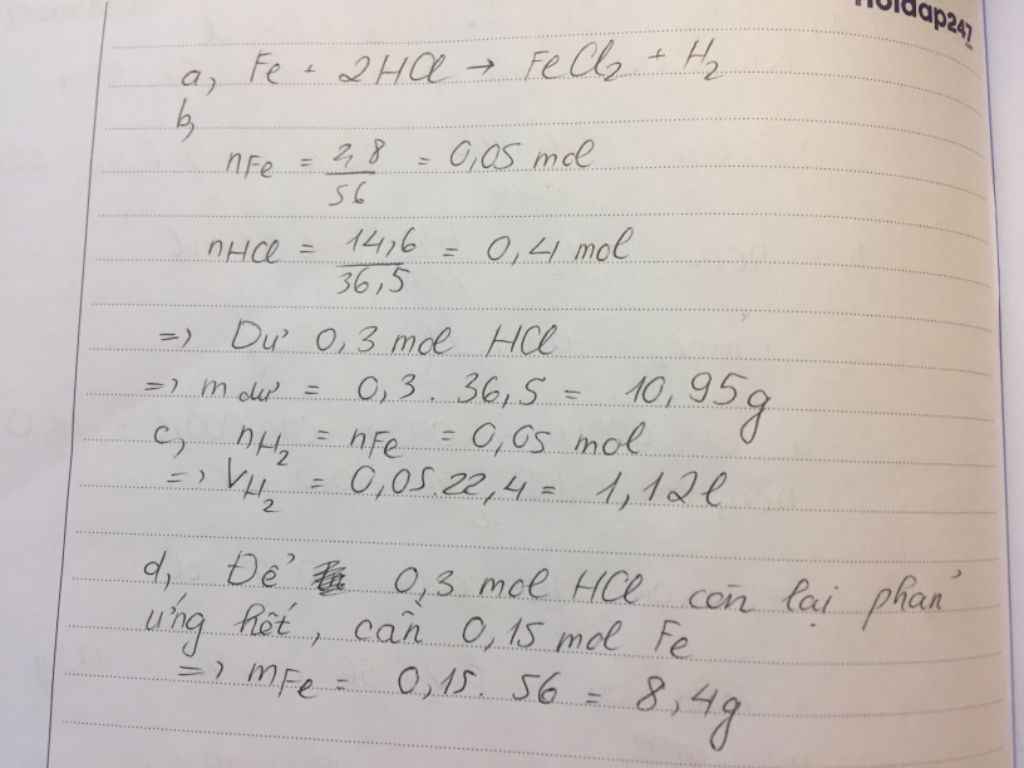

\(n_{Fe}=\dfrac{m}{M}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
1 : 2 : 1 (mol)
0,05 : 0,4 (mol)
-Chuyển thành tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,4}{2}\Rightarrow\) Fe phản ứng hết còn HCl dư.
-Theo PTHH: \(n_{H_2}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
b) \(n_{Fe\left(cần\right)}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(\Rightarrow n_{Fe\left(thêm\right)}=n_{Fe\left(cần\right)}-n_{Fe\left(tt\right)}=0,2-0,05=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(thêm\right)}=n.M=0,15.56=8,4\left(g\right)\)
-Theo PTHH: nH2=0,5.11=0,5(mol)nH2=0,5.11=0,5(mol)
0,5 ở đâu ra ạ?