Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
Phần bay hơi chỉ có H2O, không có ancol, đồng thời sản phẩm lại có hai muối Na nên X là este của phenol, có thể tạp chức.
![]()
Theo định luật bảo toàn khối lượng:
mmuối ![]()
Theo định luât bảo toàn nguyên tố O: nO muối = ![]()
Muối gồm hai dạng - ONa (a mol); - COONa (b mol)
Theo định luật bảo toàn nguyên tố Na và O: a + b = 0 , 06 a + 2 b = 0 , 08 . =>a = 0,04; b = 0,02.
Do đó X phải là este đơn chức của phenol 2 chức, X có dạng RC6H3(OH) - OOCR’.
Số mol chất X: nY = b = 0,02 mol => nO trong X = 0,06 mol.
Theo đinh luât bảo toàn khối lương: mX = mC + mH + mO =>nH trong X = 0,12 mol
=> nC : nH : nO = 7 : 6 : 3 =>công thức phân tử X là C7H6O3.
Có 3 công thức cấu tạo thỏa mãn với bài toán.

Đáp án: C
nNa2CO3 = 0,03 mol ; nCO2= 0,11 mol ; nH2O = 0,05 mol
A + NaOH → H2O (1)
0,04 mol
A + NaOH → hai muối natri + O2 → Na2CO3 + CO2 + H2O (2)
4,44 g
Bảo toàn nguyên tố => nNaOH = 0,06 mol
BTKL: mA + mNaOH = mH2O + m muối
=> mH2O = 0,72 g <=> nH2O = 0,04
BTKL với phản ứng đốt muối natri:
mmuối + mO2 = mNa2CO3 + mCO2 + mH2O

nNa2CO3 = 0,03; nCO2 = 0,11;
nH2O (2) = 0,05
![]() nC = 0,14
nC = 0,14
Bảo toàn Na
![]() nNaOH = 2nNa2CO3 = 0,06
nNaOH = 2nNa2CO3 = 0,06
BTKL
![]() mH2O (1) = 2,76 + 0,06.40 – 4,44 = 0,72g
mH2O (1) = 2,76 + 0,06.40 – 4,44 = 0,72g
![]() nH2O (1) = 0,04
nH2O (1) = 0,04
Bảo toàn H
![]() nH trong X = 2nH2O – nNaOH
nH trong X = 2nH2O – nNaOH
= 2.(0,05 + 0,04) – 0,06 = 0,12
Bảo toàn khối lượng
![]() mO = 2,76 – 0,14.12 – 0,12 = 0,96g
mO = 2,76 – 0,14.12 – 0,12 = 0,96g
![]() %mO = 34,78%
%mO = 34,78%
Chọn D.

Đáp án A
nH2O = 0,1 mol
nNa2CO3 = 0,075 mol; nCO2 = 0,325 mol; nH2O = 0,175 mol.
nNaOH = 2 x nNa2CO3 = 2 x 0,075 = 0,15 mol.
nC trong X = nNa2CO3 + nCO2 = 0,075 + 0,325 = 0,4 mol.
Bảo toàn H trong X: nH trong X = 0,1 x 2 + 0,175 x 2 - 0,15 = 0,4.
Theo BTKL: a = 11,8 + 1,8 - 0,15 x 40 = 7,6 gam
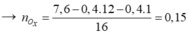
Giả sử X là CxHyOz
Vậy x : y : z = 0,4 : 0,4 : 0,15 = 8 : 8 : 3
Vậy CTĐGN của X là C8H8O

Chọn D.
Khi cho 8,28 gam A tác dụng với NaOH thì:
![]()
Khi đốt hỗn hợp rắn khan thì:
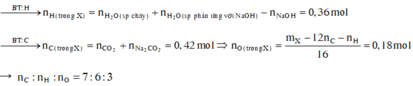
Theo đề A có CTPT trùng với CTĐG nhất của A nên CTPT của A là C 7 H 6 O 3
Nhận thấy rằng 
Phương trình phản ứng:
![]()
Cho hỗn hợp rắn qua H2SO4 dư thu được HCOOH (X) và C6H4(OH)2 (Y). Số nguyên tử H trong Y là 6.

Đáp án C
Gọi số mol H 2 O sinh ra trong phản ứng thủy phân và phản ứng đốt cháy lần lượt là n H 2 O 1 và n H 2 O 2 . Áp dụng bảo toàn nguyên tố Na cho toàn bộ quá trình phản ứng và bảo toàn khối lượng trong phản ứng của X với NaOH, ta có :
n NaOH = 2 n Na 2 CO 3 = 2 . 6 , 36 : 106 = 0 , 12 m X ⏟ 6 , 08 + m NaOH ⏟ 0 , 12 . 40 = m muối ⏟ 9 , 44 + 18 n H 2 O ( 1 ) ⏟ ?
n H 2 O 1 = 0,08
Theo bảo toàn nguyên tố C, H và giả thiết, ta có
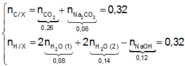
![]()
= 0,12 mol
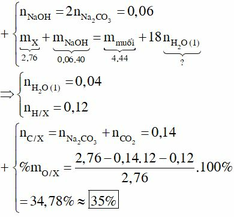

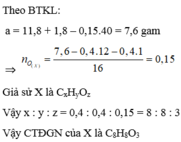
Phần bay hơi chỉ có nước, không có ancol đồng thời sản phẩm lại có 2 muối Na nên X là este của phenol, có thể có tạp chức.
Bảo toàn khối lượng, ta có:
Bảo toàn nguyên tố O có:
Muối gồm 2 dạng: -ONa (x mol) à -COONa (y mol). Bảo toàn Na và O
Do đó X phải là este đơn chức của phenol 2 chức. X có dạng R'-C6H3(OH)- OOCR
Có: nX = y = 0,02(mol) ⇒ nO trong X =0,06(mol)
Bảo toàn khối lượng: mX = mC + mO + mH
nH trong X = 0,12 ⇒ nC: nH: nO =7:6:3 ⟹ C7H6O3
Ta viết được 3 công thức cấu tạo thỏa mãn bài toán.
Đáp án C