Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
![]()
Vì sau phản ứng còn dư kim loại nên trong dung dịch B tồn tại Fe(NO3)2. Các phản láng xảy ra:
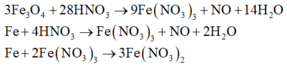
Như vậy trong toàn bộ các quá trình, số oxi hóa của sắt trong Fe và Fe3O4 đều về số oxi hóa +2.

Theo định luật bảo toàn mol electron, ta có:
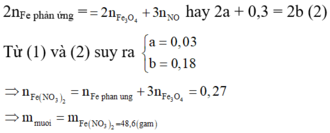

Đáp án A
Do Fe dư nên chỉ tạo ra Fe2+.
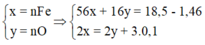
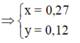
4H+ + NO3- + 3e → NO + 2H2O
2H+ + O + 2e → H2O
=> nHNO3 = nH+ = 4nNO + 2nO = 4.0,1 + 2.0,12 = 0,64
=> [HNO3] = 0,64/0,2 = 3,2M => Chọn A.

Quy hỗn hợp X thành Fe phản ứng (a mol) và O (b mol) và 1,46 g Fe không tan
Bảo toàn khối lượng => 56a + 16b + 1,46 = 18,5

Đáp án B

Quy đổi X thành các đơn chất: Cu (x mol); Fe (l,5y mol); O2 (y mol) => 64x + 116y = 61,2 - 2,4 = 58,8
Bảo toàn electron ta có: ne cho = ne nhận
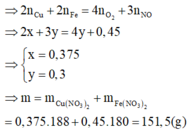
Đáp án B

Đáp án A:
nNO = 0,15 (mol), kim loại còn lại sau phản ứng là Cu.
nCu dư =0,0375(mol)
nX phản ứng= 61,2 - 2,4 = 58,8 (g)
Đặt x và y lần lượt là số mol Cu và Fe3O4.
Quy Fe3O4 thành hỗn hợp FeO và Fe2O3 có tỉ lệ mol 1:1
Theo khối lượng X => 64x+232y = 58,8
Bảo toàn electron ta có: ne cho= nenhận
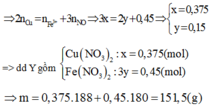

Đáp án C
Có: n FeCO 3 = n CO 2 = 0 , 03 ⇒ n Cu = 0 , 5 ( mol )
Kim loại dư nên tao thành muối Fe (II); nCu phản ứng = 0,165 (mol)
Vậy Y gồm 0,165 mol Cu(NO3)2 và 0,03 mol Fe(NO3)2
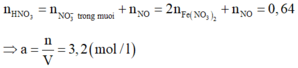
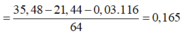
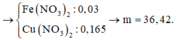
vì trong hỗn hợp còn kim loại Fe dư nên muối là Fe(NO3)2
quy đổi hỗn hợp ban đầu về hỗn hợp có x mol Fe và y mol O
(x mol Fe này là lượng Fe phản ứng không tính lượng dư, sau phản ứng klượng Fe này tạo hết thành muối nên nFe(NO3)2 = nFe = x)
⇒ 56x + 16y = 18,5 - 1,46 (1)
nNO = 2,24/22,4 =0,1
áp dụng định luật bảo toàn e
Fe → Fe+2 + 2e O +2e → O-2
x → 2x y → 2y
N+5 + 3e → N+2
0,3← 0,1
tổng số mol e nhường = tổng số mol e nhân
⇒ 2x = 2y + 0,3 (2)
từ (1) và (2) ta có
x= 0,27 ⇒nFe =0,27 ⇒ nFe(NO3)2 = 0,27 ⇒mFe(NO3)2 = 48,6 g